题目内容
10.用NaOH固体配制一定物质的量浓度的NaOH溶液时,不需要使用的玻璃仪器是( )| A. | 玻璃棒 | B. | 容量瓶 | C. | 圆底烧瓶 | D. | 胶头滴管 |
分析 用NaOH固体配制一定物质的量浓度的溶液的步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,根据配制的步骤选择使用的仪器.
解答 解:根据配制一定物质的量浓度的氢氧化钠溶液的步骤可知,配制过程中使用的仪器有:托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管等,所以选项中必须使用的仪器为容量瓶、玻璃棒、胶头滴管,而圆底烧瓶在配制中不会用到,故选C.
点评 本题考查了配制一定物质的量浓度的溶液中使用仪器选择方法,题目难度不大,注意掌握配制一定物质的量浓度的溶液步骤,能够根据配制步骤选用使用的仪器.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
1.硫酸钠是一种重要的化工原料,其溶解度曲线如图所示.下列说法正确的是( )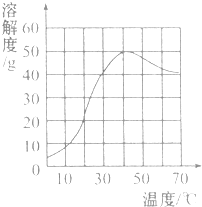

| A. | 硫酸钠的溶解度随温度升高而增大 | |
| B. | 30℃时硫酸钠饱和溶液的质量分数为40% | |
| C. | 40℃时硫酸钠的溶解度约为50g | |
| D. | 60℃时硫酸钠饱和溶液降温后一定饱和 |
18.材料是人类赖以生存和发展的重要物质基础,有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种( )
| A. | 橡胶 | B. | 纤维 | C. | 塑料 | D. | 玻璃 |
15.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| C. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2A1O2-+3H2↑ |
2.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 原子半径:A<B<C<D<E | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 金属性:D>C | |
| D. | 一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应 |
19.下列反应的离子方程式的书写正确的是( )
| A. | 锌粒与稀醋酸反应:Zn+2H+=Zn2++H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42ˉ=BaSO4↓ | |
| C. | 氯化铝溶液与过量氨水反应:Al3++3OH-=Al(OH)3↓ | |
| D. | 常温下,用氢氧化钠溶液吸收多余的氯气:Cl2+2OH-=Cl-+ClO-+H2O |
20.下列有关溶液中微粒浓度关系的叙述错误的是( )
| A. | 0.1 mol•L-1 KHC2O4溶液中:c(OH-)=c(H+)+c(H2C2O4)-c(C2O42-) | |
| B. | pH相等的①CH3COONa、②C6H5ONa、③Na2CO3、④NaOH四种溶液的物质的量浓度大小:①>②>③>④ | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 向0.1 mol•L-1 NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |