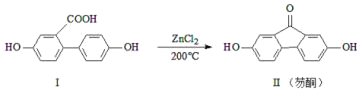
题目内容
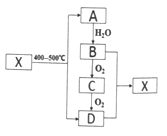
【题目】某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
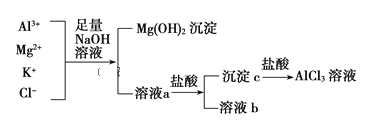
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:_________________。
(2)氢氧化钠溶液能否用氨水代替,为什么?___________________________。
(3)在溶液a中加入盐酸时需控制盐酸的量,为什么?___________。为此,改进方法是___________。
【答案】Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO![]() +2H2O 不能,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开 因为氢氧化铝能与强酸反应,所以在加入盐酸时,需要控制盐酸的量,以防止部分Al(OH)3转化成Al3+ 通入过量二氧化碳气体
+2H2O 不能,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开 因为氢氧化铝能与强酸反应,所以在加入盐酸时,需要控制盐酸的量,以防止部分Al(OH)3转化成Al3+ 通入过量二氧化碳气体
【解析】
Mg2+、K+、Al3+、Cl-的溶液中加入过量的NaOH时,生成氢氧化镁沉淀和偏铝酸根离子;则溶液a中含有K+、Al3+、Cl-、Na+、OH-、AlO2-;加入适量的盐酸,生成氢氧化铝沉淀,过滤、洗涤后,加入盐酸生成氯化铝。
(1)混合物中加入足量氢氧化钠溶液时,镁离子与氢氧根离子反应生成氢氧化镁沉淀,铝离子与氢氧根离子生成偏铝酸根离子和水,反应的离子方程式为Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO![]() +2H2O;
+2H2O;
(2)氢氧化钠溶液不能用氨水代替,因为氢氧化铝与氨水不反应,则生成的沉淀为氢氧化镁和氢氧化铝沉淀的混合物,无法分离镁离子、铝离子;
(3) 溶液a中加入盐酸需控制用量,因为过量的盐酸可与氢氧化铝反应生成氯化铝,导致得到的铝的含量降低;可以通用二氧化碳代替盐酸,因为过量二氧化碳的溶液与氢氧化铝不反应。