题目内容
【题目】二氧化硫和硫化氢都是有毒物质,但它们在工业上都有着重要的用途。请回答下列有关问题:
(1)燃煤脱疏是科研工作者研究的重要课题之一,己知有两种脱硫方法,一是活性炭作化氧化法脱流;二是CO还原法脱硫。
①活性炭在反应过程中作为催化剂,改变了______(填选项字母)。
a.反应限度 b.反应速率 c.反应活化能 d.反应焓变 e.反应路径
②CO还原法的原理是:2CO(g)+SO2(g)![]() S(g)+2CO2(g),△H。
S(g)+2CO2(g),△H。
已知:S(g)+O2(g)=SO2(g),△H1=-574.0kJ/mol,CO的燃烧热为283.0kJ/mol,则△H=___。
③在两个容积为10L的恒容绝热密闭容器中发生反应:
2CO(g)+SO2(g)![]() S(g)+2CO2(g),各起始反应物的物质的量如右表所示,起始温度均为T℃。两容器中平衡常数K甲______K乙(填“>”“=”或“<”),理由是__________。
S(g)+2CO2(g),各起始反应物的物质的量如右表所示,起始温度均为T℃。两容器中平衡常数K甲______K乙(填“>”“=”或“<”),理由是__________。

(2)H2S受热发生分解反应:2H2S(g)=2H2(g)+S2(g),在密闭容器中,充入0.20molH2S(g),压强为p时,控制不同的温度进行实验,H2S的平衡转化率如图所示。

①出强为p,温度为T6℃时,反应经tmin达到平衡,则平均反应速率v(S2)=_______mol/min.
②若压强p=aMPa,温度为T4℃时,该反应的平衡常数Kp=____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
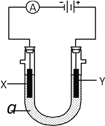
(3)H2S废气可用足量烧碱溶液吸收,将吸收后的溶液加入由惰性电极组成的电解池中进行电解,阳极区可生成Sx2-。请写出生成Sx2-的电极反应式____________。
【答案】 bce +8.0kJ/mol < 该反应的正反应为吸热反应,甲、乙相比,甲的正向进行程度大,吸牧的热量多,温度低,则K甲<K乙 0.05/t ![]() xS2--2(x-1)e-=Sx2-
xS2--2(x-1)e-=Sx2-
【解析】(1)①活性炭在反应过程中作为催化剂,改变了反应速率、反应活化能、反应路径;不能改变反应的反应限度和反应焓变;正确选项bce。
②S(g)+O2(g)=SO2(g) △H1=-574.0kJ/mol,②CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJmol-1,将②×2-①得:2CO(g)+SO2(g)![]() S(g)+2CO2(g) △H=2×(-283.0kJmol-1)-(-574.0kJ/mol)= +8.0kJ/mol;正确答案:+8.0kJ/mol;
S(g)+2CO2(g) △H=2×(-283.0kJmol-1)-(-574.0kJ/mol)= +8.0kJ/mol;正确答案:+8.0kJ/mol;
③2CO(g)+SO2(g)![]() S(g)+2CO2(g),△H=+8.0kJ/mol,该反应为吸热反应,在恒容绝热密闭容器中发生反应,甲、乙相比,甲的正向进行程度大,吸牧的热量多,温度低,向右进行的程度小,因此K甲<K乙;正确答案:<;该反应的正反应为吸热反应,甲、乙相比,甲的正向进行程度大,吸牧的热量多,温度低,则K甲<K乙。
S(g)+2CO2(g),△H=+8.0kJ/mol,该反应为吸热反应,在恒容绝热密闭容器中发生反应,甲、乙相比,甲的正向进行程度大,吸牧的热量多,温度低,向右进行的程度小,因此K甲<K乙;正确答案:<;该反应的正反应为吸热反应,甲、乙相比,甲的正向进行程度大,吸牧的热量多,温度低,则K甲<K乙。
(2)①在密闭容器中,充入0.20molH2S(g),发生2H2S(g)=2H2(g)+S2(g)反应,进行到T6℃时,硫化氢的转化率为50%,因此H2S的消耗量为0.20×50%=0.10 mol,生成S2(g)的量为1/2×0.10=0.05 mol,反应经tmin达到平衡,则平均反应速率v(S2)=0.05/tmol/min;正确答案:0.05/t。
②发生2H2S(g)=2H2(g)+S2(g)反应,温度为T4℃时,硫化氢的转化率为40%,H2S的消耗量为0.20×40%=0.08 mol,剩余硫化氢的量为2-0.08=0.12 mol,生成H2的量为0.08 mol,生成S2的量为0.04 mol,则若压强p=aMPa时,硫化氢的分压为a/2,H2的分压为a/3,S2的分压为a/6,该反应的平衡常数Kp=(a/3)2×a/6/ (a/2)2=![]() ;正确答案:
;正确答案:![]() 。
。
(3)H2S电解,阴极上氢离子放电生成氢气,阳极S2-失电子发生氧化反应生成Sx2-,极反应式为xS2--2(x-1)e-=Sx2-;正确答案:x-2(x-1)e-=Sx2-。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案