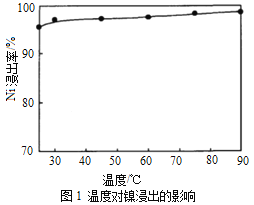
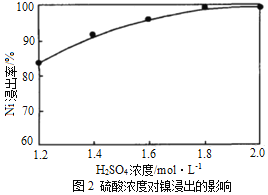
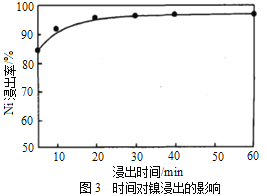
��Ŀ����
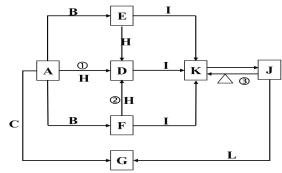
����Ŀ�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
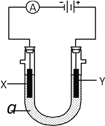
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
����X�������۲쵽��������________________________����
��Y�缫�ϵĵ缫��ӦʽΪ________________________������õ缫��Ӧ����ķ�����_____________________________________��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ�����__________���缫��Ӧʽ��_______________________________________����
��Y�缫�IJ�����__________���缫��Ӧʽ��_______________________________________����˵�������ʷ����ĵ缫��Ӧ����д����
���𰸡� �����ݣ���Һ��� 2Cl--2e-==Cl2�� ��ʪ��ĵ���KI��ֽ����Y����������ֽ������˵��Y������ΪCl2 ��ͭ Cu2++2e-==Cu ��ͭ Cu-2e-==Cu2+
����������1������X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��XΪ�������缫�������ӷŵ������������缫��ӦʽΪ2H++2e-=H2����ͬʱ�õ缫�����������������ӣ�������̪��Һ���죻��Y�缫�������ӷŵ������������缫��ӦʽΪ2Cl--2e-==Cl2�����������������ԣ����������������ɵⵥ�ʣ�����������Һ����ɫ����������������ʪ��ĵ��۵⻯����ֽ���飬����ʪ��ĵ���KI��ֽ����Y����������ֽ������˵��Y������ΪCl2����2������Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ������Ӧ���Ǵ�ͭ�������Ǵ�ͭ����X�缫�Ǵ�ͭ�������缫��ӦʽΪCu2++2e-==Cu����Y�缫�Ǵ�ͭ���缫��ӦʽΪCu-2e-==Cu2+��

����Ŀ��ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ��������д���пհף�
��1����ͼ��______������A������B�����Ǽ�ʽ�ζ��������и�ʵ��ĵ�һ��������____________________��
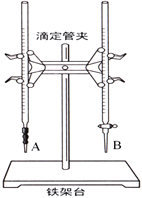
��2���ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע����ƿ����Һ��ɫ�仯��ֱ�������һ���������_____________________________��������������˵���ﵽ�ζ��յ㡣
��3�����в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵�����____��
A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B���ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
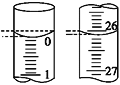
��4�����ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ��������������Һ�����Ϊ________mL��
��5��ijѧ������3��ʵ��ֱ��¼�й��������±���
�ζ����� ����NaOH��Һ�����/mL | 0.100 0 mol��L��1��������/mL | ||
�ζ�ǰ�̶� | �ζ���̶� | ||
��һ�� | 25.00 | 0.00 | 26.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 |
������ | 25.00 | 0.22 | 26.31 |
�����ϱ�������ʽ������NaOH��Һ�����ʵ���Ũ�ȣ�д����Ҫ���̣���______________