��Ŀ����
����Ŀ��ҳ�����Ǵ�ҳ�Ҳ��п��ɵ�һ�ַdz���Ҫ����Ȼ����Դ,ҳ��������Ҫ�ɷ��Ǽ���,�ǹ��ϵĽྻ��Դ��
��1��ҳ��������������ȼ��,�������������ϳ���(CO��H2)��CH4��H2O(g)ͨ��۽�̫���ܷ�Ӧ��,������ӦCH4(g)+H2O(g) = CO(g)+3H2(g)����H1����֪:CH4��H2��CO��ȼ����(��H)�ֱ�Ϊ-a kJ��mol-1��-b kJ��mol-1��-c kJ��mol-1;H2O(l)=H2O(g)����H=+d kJ��mol-1��
����H1=______________(�ú���ĸa��b��c��d�Ĵ���ʽ��ʾ)kJ��mol-1��
��2���úϳ������ɼ״��ķ�ӦΪCO(g)+2H2(g)![]() CH3OH(g)����H2,��10 L�����ܱ������а����ʵ���֮��1��2����CO��H2,���CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ:
CH3OH(g)����H2,��10 L�����ܱ������а����ʵ���֮��1��2����CO��H2,���CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ:

200 ��ʱn(H2)��ʱ��ı仯���±���ʾ:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
�٦�H2____(����>����<������=��)0��
��д��������ͬʱ��߷�Ӧ���ʺ�COת���ʵĴ�ʩ:_____��
������˵����ȷ����____(����ĸ)��
a.�¶�Խ��,�÷�Ӧ��ƽ�ⳣ��Խ��
b.��ƽ����ٳ���ϡ������,CO��ת�������
c.����������ѹǿ���ٱ仯ʱ,��Ӧ�ﵽ�����
d.ͼ��ѹǿ:p1<p2
��0~3 min����CH3OH��ʾ�ķ�Ӧ����v(CH3OH)=____mol��L-1��min-1��
��200 ��ʱ,�÷�Ӧ��ƽ�ⳣ��K=____��������200 ���ﵽƽ��ĺ����ܱ��������ټ���2 mol CO��4 mol H2��2 mol CH3OH,�����¶Ȳ���,��ѧƽ��____(��������������������������)�ƶ���
��3�����顢������KOH��Һ�����ȼ�ϵ�ء���״���³���5.6 L����,��õ�·��ת��1.2 mol����,������������Ϊ____��
���𰸡� -a+3b+c-d < ����H2Ũ�Ȼ�����ѹǿ cd ![]() (��0.067) 6.25 ���� 60%
(��0.067) 6.25 ���� 60%
����������1����֪����CH4��g��+2O2=CO2��g��+2H2O��l����H=��a kJmol��1����H2��g��+![]() O2��g��=H2O��l����H=��b kJmol��1����CO��g��+
O2��g��=H2O��l����H=��b kJmol��1����CO��g��+![]() O2��g��=CO2��g����H=��c kJmol��1����H2O ��l��=H2O��g����H=+dkJmol��1���ɸ�˹���ɿ�֪������3+���������ܿɵ�CH4��g��+H2O��g���TCO��g��+3H2��g��������H1=(��a+3b+c��d)kJmol��1��
O2��g��=CO2��g����H=��c kJmol��1����H2O ��l��=H2O��g����H=+dkJmol��1���ɸ�˹���ɿ�֪������3+���������ܿɵ�CH4��g��+H2O��g���TCO��g��+3H2��g��������H1=(��a+3b+c��d)kJmol��1��
��2������ͼʾ��֪�ں�ѹ�����£������¶ȵ�����CO��ת���ʽ��ͣ�˵�������¶�ƽ�������ƶ���������ӦΪ���ȷ�Ӧ����H2��0��
������Ӧ���ʵ���Ҫ��ʩ�У��¶����ߡ�ѹǿ��������Ũ�ȼ�ʹ�ô�������ƽ�������ƶ�ʱ����Ӧ���ת���ʿ����������ڸ÷�ӦΪ���ȷ�Ӧ���Ҵ�����Ӱ�컯ѧƽ����ƶ��������ԣ�����ͬʱ��߷�Ӧ���ʺ�COת���ʵĴ�ʩ������H2Ũ�ȡ�����ѹǿ��
��a����ӦCO��g��+2H2��g��CH3OH��g��������Ϊ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ����С��a����ȷ��b����ƽ����ٳ���ϡ�����壬ѹǿ����ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬b����ȷ��c����ӦCO��g��+2H2��g��CH3OH��g���ڽ��еĹ����У��ﵽƽ��ǰ���������ʵ����ڲ��ϱ仯��������������ѹǿ���ٱ仯ʱ��˵���������������ʵ������ٸı䣬��Ӧ�ﵽƽ�⣬����Ӧ�ﵽ����ȣ�c��ȷ��d����ͼʾ��֪���ں��º��ݵ������£�����ѹǿ��ƽ�����������ƶ���CO��ת��������ͼ��ѹǿp1��p2��d��ȷ������������˵����ȷ����cd��
���ɱ������ݿ�֪��3min��÷�Ӧ�ﵽƽ��״̬��
������ CO��g��+2H2��g��CH3OH��g����
��ʼŨ�ȣ�mol/L�� 0.4 0.8 0
�仯Ũ�ȣ�mol/L�� 0.2 0.4 0.2
��ʼŨ�ȣ�mol/L�� 0.2 0.4 0.2
03min������CH3OH��ʾ�ķ�Ӧ����v��CH3OH��=![]() =
=![]() molL��1min��1��
molL��1min��1��
���ɢܼ����ƽ��״̬��֪��200��ʱƽ�ⳣ��K= =
=![]() =6.25��������200��ﵽƽ��ĺ����ܱ��������ټ���2mol CO��2mol H2��2mol CH3OH����ʱ�����ʵ�Ũ��Ϊc��CO��=0.4mol/L��c��H2��=0.6mol/L��c��CH3OH��=0.4mol/L�������¶Ȳ��䣬��ѧƽ�ⲻ�䣬��ʱQc=
=6.25��������200��ﵽƽ��ĺ����ܱ��������ټ���2mol CO��2mol H2��2mol CH3OH����ʱ�����ʵ�Ũ��Ϊc��CO��=0.4mol/L��c��H2��=0.6mol/L��c��CH3OH��=0.4mol/L�������¶Ȳ��䣬��ѧƽ�ⲻ�䣬��ʱQc= =
=![]() =2.78��6.25=K�����ʱƽ��Ӧ������Ӧ�����ƶ���
=2.78��6.25=K�����ʱƽ��Ӧ������Ӧ�����ƶ���
��3�����顢������KOH��Һ�����ȼ�ϵ�أ�����CH4��ȫ������IJ���ΪK2CO3�����ԣ�1mol������ȫ��Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ8mol��ʵ�ʲ�õ�·��ת��1.2mol���ӣ���֪�μӷ�Ӧ�ļ���Ϊ![]() =0.15mol���ڱ�״������5.6L��������ʵ���Ϊ
=0.15mol���ڱ�״������5.6L��������ʵ���Ϊ![]() =0.25mol�������������Ϊ
=0.25mol�������������Ϊ![]() =60%��
=60%��

 ȫ�ܲ����ĩС״Ԫϵ�д�
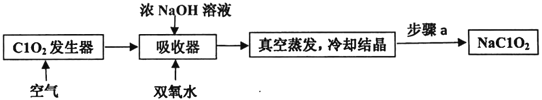
ȫ�ܲ����ĩС״Ԫϵ�д�����Ŀ�����ᾧõ�����Ǿ���ǿ��õ�������Ľᾧ�������ϣ������Ϻ����û�����Ʒ�о��й�����Ӧ�ü�ֵ���仯ѧ����Ϊ���������ȼ�����������Ŀǰ���ڹ�ҵ����Ҫʹ������·�����ϳɽᾧõ��:
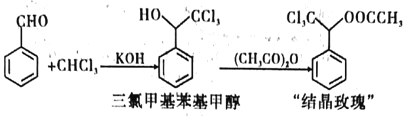
I.�ɱ���ȩ���ȷºϳ����ȼ������״���
��.���ȼ������״���������������������Ӧ�Ƶ����ᾧ��������
��֪:
���ȼ������״� | ��Է�������:225.5����ɫҺ�塣������ˮ���ܶȱ�ˮ�������Ҵ� |
������ | ��ɫҺ�塣��ˮ��Ӧ�������ᣬ�����Ҵ� |
���ᾧõ���� | ��Է�������:267.5����ɫ���塣�۵�:88����������ˮ�������Ҵ� |
����ʵ�鲽������:
I.�ɱ���ȩ���ȷºϳ����ȼ������״���
����һ:װ����ͼ��ʾ�����ν�����ȩ���ȷ¼���������ƿ��,����A�м���KOH�����ܼ����μ�A���Լ������裬��ʼ��Ӧ��������һ���¶��½��С�

�����:��Ӧ�����������������5%�����ᡢ����ˮϴ�ӡ�
������:��ϴ�Ӻ�Ļ��������ȥ�����л����ʣ�����ˮ����þ�����ˡ���Һ��Ϊ�������ȼ��ͻ��״���
��.���ȼ������״���������������������Ӧ�Ƶ����ᾧõ������
������:����һ����ƿ�м����Ʊ������ȼ������״���������������������Ũ�������Ӧ�����ȿ��Ʒ�Ӧ�¶���90�桫110��֮�䡣
������:��Ӧ��Ϻ���ӦҺ�����ˮ�У���ȴ�ᾧ������ᾧõ������
��ش���������:
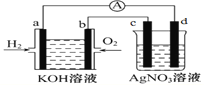
��1������A��������_________��ʵ��װ��B�У�����ˮӦ��_____�ڽ�(����a������b��)��
��2��������У���5%������ϴ�ӵ���ҪĿ����___________����ϴ�ӡ���Һ�����У�Ӧ�����Ȼ���ã����ֲ���л���Ӧ___________ (�����)��
A.ֱ�Ӵ��Ͽڵ���
B.�Ƚ�ˮ����Ͽڵ������ٽ��л�����¿ڷų�
C.ֱ�Ӵ��¿ڷų�
D.�Ƚ�ˮ����¿ڷų����ٽ��л�����¿ڷų�
��3���������У�������ˮ����þ��Ŀ����___________����δ������ˮ����þ��ֱ�ӽ������������ʽ��к�����Ӧ����ʹ���ᾧõ�����IJ���ƫ______(����������������),��ԭ����___________ (����ƽ���ƶ�ԭ������)��(��֪���ľ��巴Ӧ��ͼ��ʾ)

��4���������У�����ʱ��Ӧ�ȼ������ȼ������״�����������Ȼ����������Ũ���Ტ���裬��Ҫ��Ϊ��__________�����ȷ�Ӧʱ��Ϊ�ϺõĿ����¶ȣ������˵ļ��ȷ�ʽΪ_____(����ˮԡ������������ԡ������)��
��5��22.55g�����������״���������������ַ�Ӧ�õ��ᾧõ��21.40g,�������_____��