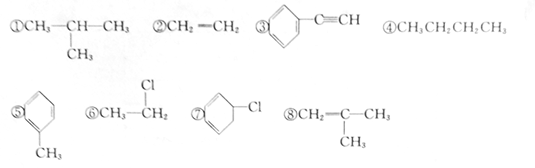
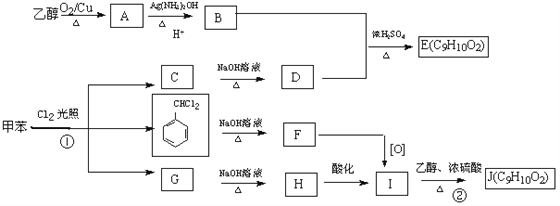
��Ŀ����
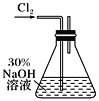
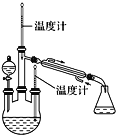
����Ŀ��������ʵ��������¹ʴ����������� ��50 mL��Ͳ��ȡ5.0 mL����ͭ��Һ���� ����û�и�ʴ�Թ���ҩƷʱ����ҩƷ���������ϳ������� ��������Ũ��Һ�����������У�Ӧ�����ô���ˮ��ϴ�����ұ�ϴ��գ�۾����� �㵹Һ��ʱ���Լ�ƿ��ƿ�ڲ��������ڣ��� ��״ҩƷ��Ҫ��ҩ��ȡ�ã��� ����ҩƷ��ϸ��ƿ���棻�� ����ͼ��ʾ�ķ������������ζ���� ��ʵ���в����ֱ��������ƣ����õ�ƻ�˫��ˮ��ϴ������ҩ��� ú���ж����ˣ����������˹��������� ŨH2SO4����Ƥ���ϣ���NaOH��Һ�к͡����д������( )
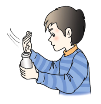
A. �٢ڢۢߢ�� B. �ۢܢ� C. �ڢݢޢߢ� D. �٢ڢܢݢޢ��
���𰸡�D
��������
����Ͳ��ȡ5mL����ͭ��ҺӦ��ѡ��10mL��Ͳ���ڸ��ݳ���û�и�ʴ�Թ���ҩƷʱ����ȷ������������ ��������Ũ��Һ�����������У�Ӧ�����ô���ˮ��ϴ�����ұ�ϴ��գ�۾�����Ӧ�ý��Լ�ƿ���������ڽ�����һ�𣻢�ȡ��״����һ��������ȡ�ã����ƿ����������壬ϸ��ƿ����Һ�壮�� ������Ƿ�����ͼ��ʾ�ķ������������ζ���� ��ʵ���в����ֱ��������ƣ����õ�ƻ�˫��ˮ��ϴ������ҩ���һ����̼�ж��������е�Ѫ�쵰��һ����̼��ϣ�ʹ��ȱ�����ж����������մ���·���Ƥ���ϣ�Ӧ����Ĩ����ȥ��Ȼ����ˮ��ϴ��
����50mL��Ͳ��ȡ5mL����ͭ��Һ�����̫����Ͳ��ȡ5mL����ͭ��Һ��Ӧ��ѡ��10mL��Ͳ���ʢٴ���
��Ӧ�������ϸ���һ��������ͬ��ֽƬ��������ȾҩƷ�������̣��ʢڴ�����
�� ��������Ũ��Һ�����������У�Ӧ�����ô���ˮ��ϴ�����ұ�ϴ��գ�۾�,�ʢ���ȷ��
���㵹Һ��ʱ��Ӧʹ�Լ�ƿ���������ڽ�����һ�𣬱���Һ�����������⣬�ʢܴ���
�ݹ���ҩƷȡ��ʱ��ȡ�÷�ĩ״������ҩ�ף���״����һ�������ӣ��ʢݴ���
��ҩƷ����ʱ��ϸ��ƿ����ϸ��ƿʢҺ�壬���ƿ������������壬�ʢ���
�� ������Ƿ�����ͼ��ʾ�ķ������������ζ���ʢ���ȷ��
�� ��ʵ���в����ֱ��������ƣ����õ�ƻ�˫��ˮ��ϴ������ҩ����Է���Ⱦ���ʢ���ȷ��
��һ����̼�ж��������е�Ѫ�쵰��һ����̼��ϣ�ʹ��ȱ�����ж�������ú���ж����ˣ�ҪѸ���ƶ�ͨ��ĵط������������˹��������ʢ����
�����մ���·���Ƥ���ϣ�Ӧ����Ĩ����ȥ��Ȼ����ˮ��ϴ��ŨNaOH����ǿ��ʴ�ԣ����Բ�����ŨNaOH��ϴ���ʢ����
��ѡD��

 �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д� �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�����Ŀ��ҳ�����Ǵ�ҳ�Ҳ��п��ɵ�һ�ַdz���Ҫ����Ȼ����Դ,ҳ��������Ҫ�ɷ��Ǽ���,�ǹ��ϵĽྻ��Դ��
��1��ҳ��������������ȼ��,�������������ϳ���(CO��H2)��CH4��H2O(g)ͨ��۽�̫���ܷ�Ӧ��,������ӦCH4(g)+H2O(g) = CO(g)+3H2(g)����H1����֪:CH4��H2��CO��ȼ����(��H)�ֱ�Ϊ-a kJ��mol-1��-b kJ��mol-1��-c kJ��mol-1;H2O(l)=H2O(g)����H=+d kJ��mol-1��
����H1=______________(�ú���ĸa��b��c��d�Ĵ���ʽ��ʾ)kJ��mol-1��
��2���úϳ������ɼ״��ķ�ӦΪCO(g)+2H2(g)![]() CH3OH(g)����H2,��10 L�����ܱ������а����ʵ���֮��1��2����CO��H2,���CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ:
CH3OH(g)����H2,��10 L�����ܱ������а����ʵ���֮��1��2����CO��H2,���CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ:

200 ��ʱn(H2)��ʱ��ı仯���±���ʾ:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
�٦�H2____(����>����<������=��)0��
��д��������ͬʱ��߷�Ӧ���ʺ�COת���ʵĴ�ʩ:_____��
������˵����ȷ����____(����ĸ)��
a.�¶�Խ��,�÷�Ӧ��ƽ�ⳣ��Խ��
b.��ƽ����ٳ���ϡ������,CO��ת�������
c.����������ѹǿ���ٱ仯ʱ,��Ӧ�ﵽ�����
d.ͼ��ѹǿ:p1<p2
��0~3 min����CH3OH��ʾ�ķ�Ӧ����v(CH3OH)=____mol��L-1��min-1��
��200 ��ʱ,�÷�Ӧ��ƽ�ⳣ��K=____��������200 ���ﵽƽ��ĺ����ܱ��������ټ���2 mol CO��4 mol H2��2 mol CH3OH,�����¶Ȳ���,��ѧƽ��____(��������������������������)�ƶ���
��3�����顢������KOH��Һ�����ȼ�ϵ�ء���״���³���5.6 L����,��õ�·��ת��1.2 mol����,������������Ϊ____��