题目内容
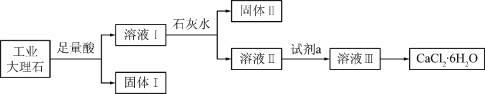
【题目】下列是部分矿物资源铝土矿(主要含有氧化铝、氧化铁)和黄铜矿(主要成分CuFeS2)的利用及产品生产流程,有关说法不正确的是( )
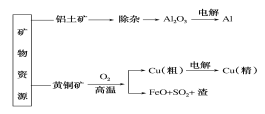
A. 除杂过程中铝元素的存在形式的变化可以如下:Al2O3→AlO2-→Al(OH)3→Al2O3
B. Al和Cu(精)均在电解槽的阴极获得
C. 粗铜炼制过程中反应2CuFeS2+O2![]() Cu2S+2FeS+SO2,每转移1.2mol电子,则有0.2mol硫被氧化
Cu2S+2FeS+SO2,每转移1.2mol电子,则有0.2mol硫被氧化
D. 若电解法分别制铝和铜的过程中转移电子数相等,理论上获得的铝和铜的物质的量之比为3:2
【答案】D
【解析】
A.铝土矿中氧化铝溶于强碱,除去氧化铁,生成偏铝酸根离子,再通入二氧化碳生成氢氧化铝,过滤、洗涤、干燥灼烧氢氧化铝生成氧化铝,除杂过程中铝元素的存在形式的变化可以如下:Al2O3→AlO2-→Al(OH)3→Al2O3,A正确;
B.Al和Cu(精)在电解精炼时,均为金属离子生成单质,则在电解槽的阴极获得,B正确;
C.粗铜炼制过程中反应2CuFeS2+O2![]() Cu2S+2FeS+SO2,Cu、O的化合价降低,部分S的化合价由-2价变为+4价,得到6个电子,则每转移1.2mol电子,则有0.2mol硫被氧化,C正确;
Cu2S+2FeS+SO2,Cu、O的化合价降低,部分S的化合价由-2价变为+4价,得到6个电子,则每转移1.2mol电子,则有0.2mol硫被氧化,C正确;
D.若电解法分别制铝和铜的过程中转移电子数相等,Al的化合价由+3变为0,Cu的化合价由+2变为0,理论上获得的铝和铜的物质的量之比为2:3,D错误;
答案为D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目