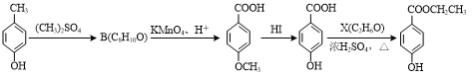
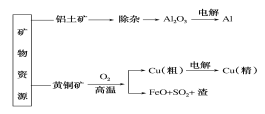
��Ŀ����
����Ŀ���������з�Ӧ��
��2H2O+Cl2+SO2��H2SO4+2HCl
��KMnO4+ HCl(Ũ)�� KCl+ MnCl2+ Cl2��+ H2O��δ��ƽ��
�������������Ӧ�ش�
��1���õ����ű�����е���ת�Ƶķ������Ŀ��д�ڴ���ϣ�_________________________
��2����ƽ��___KMnO4+___HCl(Ũ)��___KCl+___MnCl2+___Cl2��+___H2O д���ڵ����ӷ���ʽ________________________________����������ʾ��MnCl2������ˮ�������������뻹ԭ��������֮��Ϊ_____________��
��3����Ӧ�����Ȼ�����ֳ���������________________________��
��4��Cl2��SO2��KMnO4����������ǿ������˳��Ϊ__________________________��
���𰸡�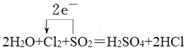 2 16 2 2 5 8 2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O 1��5 ���ԡ���ԭ�� KMnO4 >Cl2>SO2
2 16 2 2 5 8 2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O 1��5 ���ԡ���ԭ�� KMnO4 >Cl2>SO2
��������
��1�����ݻ�ԭ��ʧ���ӣ�ת�Ƹ����������е����ű�ע��ע�����������ԭ��Ӧ���ɷ�������ת�Ƶ�������
��2�����ݵ����غ㡢ԭ���غ������ƽ������������ԭ��Ӧ���ɷ����������뻹ԭ���ķ�����֮�ȣ�
��3����Ӧ�����Ȼ�������Ԫ�ز��ֻ��ϼ����ߣ����ֳ������������ԡ���ԭ�ԡ�
��4�����������ԣ���������������������з�����
��1���÷�Ӧ��SԪ�ػ��ϼ���+4�۱�Ϊ+6�ۡ�ClԪ�ػ��ϼ���0�۱�Ϊ-1�ۣ��õ����ű�����е���ת�Ƶķ������Ŀ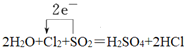 ��
��
��2���÷�Ӧ��MnԪ�ػ��ϼ���+7�۱�Ϊ+2�ۡ�����ClԪ�ػ��ϼ���-1�۱�Ϊ0�ۡ�����ClԪ�ػ��ϼ۲��䣬��ת�Ƶ�������Ϊ10����KMnO4��ϵ��Ϊ2������ϵ��Ϊ5�����ԭ���غ���ƽ����ʽΪ��2KMnO4+16HCl=2MnCl2+5Cl2��+2KCl+8H2O���ڵ����ӷ���ʽ 2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O��������������KMnO4���뻹ԭ����HCl��������֮��Ϊ2:10=1:5��
��3����Ӧ�����Ȼ�����ֳ������������ԡ���ԭ�ԣ�
��4��������ԭ��Ӧ����������������ǿ����������ɢ������ԣ�Cl2>SO2���ɢ������ԣ�KMnO4 >Cl2��Cl2��SO2��KMnO4����������ǿ������˳��Ϊ KMnO4 >Cl2>SO2��

����Ŀ��(1)��֪Ksp[Cu(OH)2]��2.2��10��20��Ksp[Fe(OH)3]��2.6��10��39�������£�ij����CuCl2��Һ�к���������FeCl3��Ϊ�˵õ�������CuCl2��2H2O���壬Ӧ����___________(��������Ļ�ѧʽ)��������Һ��pH��4��ʹ��Һ�е�Fe3��ת��ΪFe(OH)3��������ʱ��Һ�е�c(Fe3��)��________�����˺�������Һ����������Ũ���ᾧ���ɵõ�CuCl2��2H2O���塣
(2)ij̼�ظֹ�¯��ˮ������Ҫ�ɷ���̼��ơ�����ơ�������þ�����⡢��������ȡ�ˮ���輰ʱ��ϴ��ȥ����ϴ�������£�
��.����NaOH��Na2CO3���Һ�����ȣ�������Сʱ��
��.�ų�ϴ�ӷ�Һ����ˮ��ϴ��¯������ϡ���������NaF��Һ�����ݣ�
��.��ϴ��Һ�м���Na2SO3��Һ��
��.��ϴ��꣬��NaNO2��Һ�ۻ���¯��
����ϡ�����ܽ�̼��Ƶ����ӷ���ʽ��_____________________________��
����֪��25 ��ʱ�й����ʵ��ܶȻ�
���� | CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
Ksp | 2.8��10��9 | 9.1��10��6 | 1.8��10��11 | 6.8��10��6 |
�������ݣ���ϻ�ѧƽ��ԭ��������ϴCaSO4�Ĺ���________________�������ܽ�ƽ�����ʽ�ͱ�Ҫ��������������˵�������ڲ������ݹ����л��ᷢ����ӦMgCO3(s)��2OH��(aq)![]() Mg(OH)2(s)��CO32-(aq)���÷�Ӧ��ƽ�ⳣ��K��________(������λ��Ч����)��
Mg(OH)2(s)��CO32-(aq)���÷�Ӧ��ƽ�ⳣ��K��________(������λ��Ч����)��
�۲�����У�����Na2SO3��Һ��Ŀ����_______________________________��
����Ŀ��t ��ʱ�������������ܱ������з�����Ӧ��X(g)+3Y(g)![]() 2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±�������˵����ȷ����
2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±�������˵����ȷ����
���� | X | Y | Z |
��ʼŨ��/mol��L-1 | 0.1 | 0.2 | 0 |
2 minĩŨ��/mol��L-1 | 0.08 | a | b |
ƽ��Ũ��/mol��L-1 | 0.05 | 0.05 | 0.1 |
A. ƽ��ʱ��X��ת����Ϊ20%
B. t ��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ40
C. ǰ2 min�ڣ���Y�ı仯����ʾ��ƽ����Ӧ����v(Y)="0.03" mol��L-1��min-1
D. ����ƽ������ϵѹǿ��v������v����С��ƽ��������Ӧ�����ƶ�