题目内容
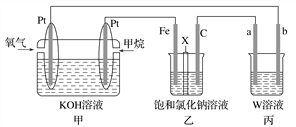
【题目】如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极 上析出6.4g某金属,下列说法正确的是
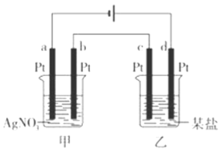
A.甲池是b极上析出金属银,乙池是c极上析出某金属
B.甲池是a极上析出金属银,乙池是d极上析出某金属
C.某盐溶液可能是CuSO4溶液
D.某盐溶液可能是Mg(NO3)2溶液
【答案】C
【解析】
甲池中a极与电源负极相连为阴极,电极上银离子得电子析出银单质,b电极为阳极,水电离出的氢氧根放电产生氧气,同时产生氢离子;乙池中c为阴极,d为阳极,乙池电极析出6.4g金属,金属应在c极析出,说明乙池中含有氧化性比氢离子强的金属阳离子。
A.甲池a极上析出金属银,乙池c极上析出某金属,故A错误;
B.甲池a极上析出金属银,乙池c极上析出某金属,故B错误;
C.乙池电极析出6.4g金属,说明乙池中含有氧化性比氢离子强的金属阳离子,Cu2+氧化性强于氢离子,会先于氢离子放电,则某盐溶液可能是CuSO4溶液,故C正确;
D.Mg2+氧化性较弱,电解时在溶液中不能得电子析出金属,所以某盐溶液不能是Mg(NO3)2溶液,故D错误;
故答案为C。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目