题目内容
【题目】一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
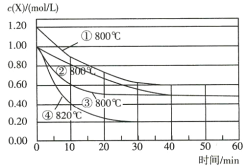
(1)该反应的平衡常数表达式K=__;根据图,升高温度,K值将__(填“增大”、“减小”或“不变”)。

(2)500℃时,从反应开始到化学平衡状态,以H2的浓度变化表示的化学反应速率是__(用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是__(填字母,下同)。
a.υ生成(CH3OH)=υ消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的![]() ,在其他条件不变的情况下,对平衡体系产生的影响是____。
,在其他条件不变的情况下,对平衡体系产生的影响是____。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时![]() 减小
减小
【答案】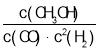 减小
减小 ![]() mol·L-1·min-1 cd cd
mol·L-1·min-1 cd cd
【解析】
由方程式可得反应平衡常数K=![]() ,根据所给图像判断出正反应为放热反应,逆反应为吸热反应,由于υ(CH3OH)∶υ(H2)=1∶2,因此可先求出υ(CH3OH),再推算出υ(H2)。根据化学平衡的标志和压强对化学平衡的影响进行解答。
,根据所给图像判断出正反应为放热反应,逆反应为吸热反应,由于υ(CH3OH)∶υ(H2)=1∶2,因此可先求出υ(CH3OH),再推算出υ(H2)。根据化学平衡的标志和压强对化学平衡的影响进行解答。
(1)由方程式可得反应平衡常数K=![]() ,根据所给图像判断,500℃时CH3OH的物质的量比300 ℃时CH3OH的量少,说明升高温度平衡逆向移动,K值减小。
,根据所给图像判断,500℃时CH3OH的物质的量比300 ℃时CH3OH的量少,说明升高温度平衡逆向移动,K值减小。
故答案为![]() 减小
减小
(2)根据图像υ(CH3OH)= ![]() mol·L-1·min-1,由于υ(CH3OH)∶υ(H2)=1∶2,则υ(H2) =
mol·L-1·min-1,由于υ(CH3OH)∶υ(H2)=1∶2,则υ(H2) =![]() mol·L-1·min-1 。
mol·L-1·min-1 。
故答案为![]() mol·L-1·min-1
mol·L-1·min-1
(3)a项,均为正反应方向的反应速率,故不能说明反应达到平衡状态;b项,由于气体的总质量为定值,且容器的体积保持不变,故密度一直不变,密度不再变化不能说明反应达到平衡状态;c项,由于气体的总质量为定值,建立平衡过程中混合气的物质的量变化,混合气的平均相对分子质量变化,混合气的平均相对分子质量不再变化能说明反应达到平衡状态;d项,CO、H2、CH3OH的浓度不再变化是平衡状态的特征标志。
故答案为cd;
(4)体积压缩,即增大压强,平衡右移;a项,由于体积减小,各物质的物质的量浓度均增加,c(H2)增大;b项,正、逆反应速率均加快;c项,增大压强,平衡右移,CH3OH物质的量增大;d项,增大压强,平衡右移,H2物质的量减小,CH3OH物质的量增大,由于![]() =
=![]() ,故
,故![]() 减小。
减小。
故答案为cd。