题目内容
【题目】T℃时,将2.0molA(g)和2.0molB(g)充入体积为1L的密闭容器中,在一定条件发生下述反应:A(g)+B(g)![]() 2C(g)+D(s) △H<0;t时刻反应达到平衡时,C(g)为2.0mol。下列说法正确的是( )
2C(g)+D(s) △H<0;t时刻反应达到平衡时,C(g)为2.0mol。下列说法正确的是( )
A.t时刻反应达到平衡时,A(g)的体积分数为20%
B.T℃时该反应的化学平衡常数K=2
C.t时刻反应达到平衡后,缩小容器体积,平衡逆向移动
D.T℃时,若将A(g)、B(g)各1.0mol充入同样容器,平衡后,a(A)为50%
【答案】D
【解析】
t时刻反应达到平衡时,C(g)为2.0mol,则

A.t时刻反应达到平衡时,A(g)的体积分数为![]() ×100%=25%,故A错误;
×100%=25%,故A错误;
B.T℃时该反应的化学平衡常数Kc=![]() =4,故B错误;
=4,故B错误;
C.反应前后体积不变,增大压强,平衡不移动,故C错误;
D.相同条件下,若将1.0molA(g)和1.0molB(g)充入同样容器,达到平衡后,假设A的转化率为x,则

则![]() =4,x=0.5,A(g)的转化率为50%,故D正确;
=4,x=0.5,A(g)的转化率为50%,故D正确;
故选D。

【题目】工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶性杂质)回收铜和铬等金属,回收流程如图所示:
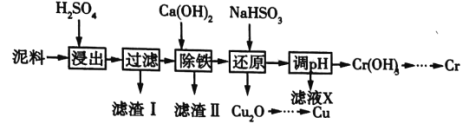
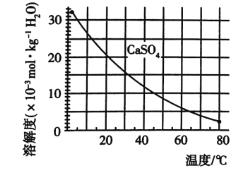
已知部分物质沉淀的pH(如表)及CaSO4元的溶解度曲线(如图):
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀 | 2.1 | 4.7 | 4.3 |
完全沉淀 | 3.2 | 6.7 | 5.6 |
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有_____________(填化学式)。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH到______;
②将浊液加热到80℃,____________。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子方程式:_________,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是______________。