题目内容
【题目】2019年诺贝尔化学奖花落锂离子电池,美英日三名科学家获奖,他们创造了一个可充电的世界。像高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。

原理如下:(1x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC。下列说法不正确的是( )
LiFePO4+nC。下列说法不正确的是( )
A.放电时,正极电极反应式:xFePO4+xLi++xe-=xLiFePO4
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式:xLi++xe-+nC=LixCn
D.充电时,Li+向左移动
【答案】D
【解析】
放电为原电池原理,从(1x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC可知,LixCn中的C化合价升高了,所以LixCn失电子,作负极,那么负极反应为:
LiFePO4+nC可知,LixCn中的C化合价升高了,所以LixCn失电子,作负极,那么负极反应为:![]() +nC,LiFePO4作正极,正极反应为:
+nC,LiFePO4作正极,正极反应为:![]() ,充电为电解池工作原理,反应为放电的逆过程,据此分析解答。
,充电为电解池工作原理,反应为放电的逆过程,据此分析解答。
A.由以上分析可知,放电正极上![]() 得到电子,发生还原反应生成
得到电子,发生还原反应生成![]() ,正极电极反应式:
,正极电极反应式:![]() ,A正确;
,A正确;
B.原电池中电子流向是负极![]() 导线
导线![]() 用电器
用电器![]() 导线
导线![]() 正极,放电时,电子由负极经导线、用电器、导线到正极,B正确;
正极,放电时,电子由负极经导线、用电器、导线到正极,B正确;
C.充电时,阴极为放电时的逆过程,![]() 变化为
变化为![]() ,电极反应式:
,电极反应式:![]() ,C正确;
,C正确;
D.充电时,作为电解池,阳离子向阴极移动,![]() 向右移动,D错误;
向右移动,D错误;
答案选D。

【题目】氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题。
I.NOx和SO2在空气中存在下列平衡:
2NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1
2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1
SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3.
(1)写出NO2和SO2反应的热化学方程式为_________.
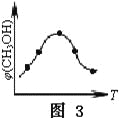
(2)随温度升高,该反应化学平衡常数变化趋势是_____.
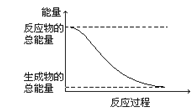
II.(1)目前,应用NH3的催化还原法来进行烟气氮氧化物脱除,化学反应可表示为:2NH3(g)+NO(g)+NO2(g)== 2N2(g)+3H2O(g) △H<0,该反应中,反应物总能量_____(填“>”、“<”或“=”)生成物总能量。
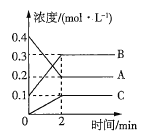
(2)已知4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) ΔH=-1800 kJ·mol-1,将2 mol NH3、3 mol NO的混合气体分别置于a、b、c三个10 L恒容密闭容器中,使反应在不同条件下进行,反应过程中c(N2)随时间的变化如图所示。
5N2(g)+6H2O(g) ΔH=-1800 kJ·mol-1,将2 mol NH3、3 mol NO的混合气体分别置于a、b、c三个10 L恒容密闭容器中,使反应在不同条件下进行,反应过程中c(N2)随时间的变化如图所示。
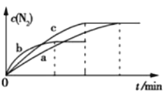
①与容器a中的反应相比,容器b中的反应改变的实验条件可能是_______,判断的依据是___________________。
②一定温度下,下列能说明反应已达到平衡状态的是____
A.H2O(g)与NO的生成速率相等 B.混合气体的密度保持不变
C.ΔH保持不变 D.容器的总压强保持不变
(3)用NH3和Cl2反应可以制备具有强氧化性的三氯胺(三氯胺在中性、酸性环境中会发生强烈水解,生成具有强杀菌作用的物质),方程式为3Cl2(g)+NH3(g)![]() NCl3(l)+3HCl(g),向容积均为1L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2molCl2和2molNH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
NCl3(l)+3HCl(g),向容积均为1L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2molCl2和2molNH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
t /min | 0 | 40 | 80 | 120 | 160 |
n(Cl2)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(Cl2)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①T℃__________400℃(填“>”或“<”)。
②该反应的ΔH__________0(填“>”或“<”)。
③该反应自发进行的条件是__________(填高温、低温、任何温度)。
④对该反应,下列说法正确的是_________(填选项字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.若容器内Cl2和NH3物质的量之比为3∶1,则表明反应达到平衡状态
C.反应达到平衡后,其他条件不变,在原容器中按![]() 继续充入一定量反应物,达新平衡后Cl2的转化率增大
继续充入一定量反应物,达新平衡后Cl2的转化率增大
D.反应达到平衡后,其他条件不变,加入一定量的NC13,平衡将向逆反应方向移动
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示![]() 省略夹持和净化装置
省略夹持和净化装置![]() 仅用此装置和表中提供的物质完成相关实验,最合理的选项是
仅用此装置和表中提供的物质完成相关实验,最合理的选项是
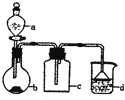
选项 | a中的物质 | b中的物质 | c中的物质 | d中的物质 |
A | 浓氨水 | NaOH |
|
|
B | 浓盐酸 |
|
| NaOH溶液 |
C | 稀硝酸 | Cu | NO |
|
D | 浓硫酸 |
|
| NaOH溶液 |
A.AB.BC.CD.D