题目内容
19.在常温常压下,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ/mol自发进行的原因是( )| A. | 吸热反应 | B. | 放热反应 | ||
| C. | 熵减反应 | D. | 熵增效应大于能量效应 |
分析 反应能否自发进行取决于焓变和熵变的综合判据:△H-T•△S<0,据此解答.
解答 解:反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ/mol是熵增加的,吸热的反应,根据△G=△H-T•△S判断,反应能自发进行,必须满足△H-T•△S<0才可,即熵增大效应大于能量效应,
故选:D.
点评 本题考查了反应能够自发进行的判断依据,解题时注意反应能否自发进行,不取决于焓变或熵变中的一种,而是二者的综合判据,当△H-T•△S<0时,反应才能自发进行,题目难度不大.

练习册系列答案
相关题目
2.下列各组物质发生状态变化时,所克服的微粒间的相互作用,属于同种类型的是( )
| A. | 钠和硫的熔化 | B. | 食盐和石蜡的熔化 | ||
| C. | 碘和干冰的升华 | D. | 二氧化硅和氧化钠的熔化 |
7.下列说法中正确的是( )
| A. | 冰融化时,分子中氢氧键发生断裂 | |
| B. | 原子晶体中共价键越强,熔点和沸点越高 | |
| C. | 分子晶体中共价键键能越大,该分子晶体的熔点和沸点一定也越高 | |
| D. | 分子晶体中分子间作用力越大,该物质越稳定 |
14.下列各组物质,化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同的( )
| A. | HCl KCl | B. | CO2 SiO2 | C. | NH4Cl CCl4 | D. | NaOH Na2O2 |
11.下列有关油脂的叙述中,不正确的是( )
| A. | 油脂没有固体的熔点,因为油脂是混合物 | |
| B. | 油脂是由高级脂肪酸和甘油所生成的酯 | |
| C. | 油脂可以在酸性或碱性条件下水解 | |
| D. | 油脂都不能使溴水褪色 |
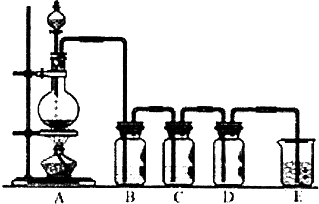 (1)若利用如图装置制备纯净、干燥的氯气,装置A中反应的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.则装置B中的液体是饱和NaCl溶液;装置C中试剂的作用是干燥氯气
(1)若利用如图装置制备纯净、干燥的氯气,装置A中反应的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.则装置B中的液体是饱和NaCl溶液;装置C中试剂的作用是干燥氯气