题目内容
14.下列各组物质,化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同的( )| A. | HCl KCl | B. | CO2 SiO2 | C. | NH4Cl CCl4 | D. | NaOH Na2O2 |
分析 一般来说,活泼金属和活泼非金属元素之间存在离子键、非金属元素之间存在共价键,分子晶体和原子晶体中存在共价键、离子晶体中存在离子键,分子晶体熔化时破坏分子间作用力、原子晶体熔化时破坏共价键、离子晶体熔化时破坏离子键.
解答 解:A.HCl中只含共价键,为分子晶体,熔化时破坏分子间作用力,KCl中只含离子键,为离子晶体,熔化时只破坏离子键,所以二者不同,故A错误;
B.CO2、SiO2中都只含共价键,CO2为分子晶体、SiO2为原子晶体,CO2固体熔化时破坏分子间作用力、SiO2熔化时破坏共价键,所以二者不同,故B错误;
C.NH4Cl中含有离子键和共价键,CCl4中只含共价键,所以熔化时,氯化铵破坏离子键、四氯化碳破坏分子间作用力,所以二者不同,故C错误;
D.NaOH、Na2O2中都含有离子键和共价键,都属于离子晶体,熔化时二者都破坏离子键,所以二者化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同,故D正确;
故选D.
点评 本题考查了化学键、晶体类型及熔化时破坏的作用力,根据晶体类型确定熔化时破坏的作用力,注意:二氧化硅和二氧化碳虽然都只含共价键,但因为晶体类型不同,导致熔化时破坏的作用力不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.SO2是造成大气污染的主要气体,造成大气中SO2含量增加最主要原因是( )
| A. | 实验室排放的SO2 | B. | 火山爆发产生的SO2 | ||
| C. | 燃烧煤和石油产品产生的SO2 | D. | 工业制硫酸排放的SO2 |
5.某化合物在核磁共振氢谱中出现5个峰,其结构简式可能是( )
| A. | 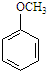 | B. |  | C. | 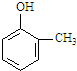 | D. | 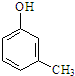 |
9.把m mol C2H4和n mol氢气混合于密闭容器中,在适当的条件下生成了p mol C2H6,若将所得的混合气体完全燃烧生成二氧化碳和水,则需氧气( )
| A. | 3.5p mol | B. | (3m+n/2)mol | C. | (3m+n)mol | D. | (3m+n/2-3 p)mol |
19.在常温常压下,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ/mol自发进行的原因是( )
| A. | 吸热反应 | B. | 放热反应 | ||
| C. | 熵减反应 | D. | 熵增效应大于能量效应 |
6.下列各组物质中,按单质、化合物、混合物顺序排列的是( )
| A. | 铁、四氧化三铁、冰水混合物 | B. | 金属钙、氧化钙、石灰水 | ||
| C. | 水银、空气、干冰 | D. | 二氧化硫、水蒸气、天然气 |
4.下列说法错误的是( )
| A. | 烧碱是强电解质,在水溶液中完全电离 | |
| B. | 将水加热,水的电离平衡向正反应方向移动,Kw变大 | |
| C. | 向溶液中加酸、加碱都能抑制水的电离 | |
| D. | 根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |