题目内容
4.等质量的下列有机物完全燃烧,消耗O2最多的是( )| A. | CH4 | B. | CH2=CH2 | C. |  | D. | CH3CH2OH |
分析 CH3CH2OH可以改写为C2H4.H2O,等质量的CH3CH2OH与C2H4对比,C2H4的耗氧量较大,而等质量的烃燃烧,耗氧量取决于H%,H%越大耗氧量越大,据此判断.
解答 解:CH4中N(C):N(H)=1:4,CH2=CH2中N(C):N(H)=1:2, 中N(C):N(H)=1:1,三者中CH4的H的质量分数最大,三者相同质量时,CH4的耗氧量最大,而CH3CH2OH可以改写为C2H4.H2O,等质量的CH3CH2OH与C2H4对比,C2H4的耗氧量较大,故CH4的耗氧量最大,故选A.
中N(C):N(H)=1:1,三者中CH4的H的质量分数最大,三者相同质量时,CH4的耗氧量最大,而CH3CH2OH可以改写为C2H4.H2O,等质量的CH3CH2OH与C2H4对比,C2H4的耗氧量较大,故CH4的耗氧量最大,故选A.
点评 本题考查化学方程式有关计算,注意根据相同质量的C、H消耗氧气的质量,确定烃中H的质量分数越大耗氧量越大,注意利用改写法将含氧衍生物转化为烃进行比较,侧重考查学生分析计算能力.

练习册系列答案
相关题目
14.在25℃水中加入下列物质,不会使水的电离平衡发生移动的是( )
| A. | KI | B. | 浓氨水 | C. | 冰醋酸 | D. | 热水 |
15.下列物质易溶于水的是( )
| A. | 葡萄糖 | B. | 油脂 | C. | 苯 | D. | 乙烯 |
19.a、b、c、d、e、f、g为七种由短期周期元素构成的粒子,它们都有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可反应生成两个共价型g分子.
试写出:
(1)d分子的空间构型为三角锥形.
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:NaOH>Mg(OH)2 (用化学式表示).
(3)d溶于水的电离方程式NH3+H2O?NH3•H2O?NH4++OH-.
(4)g粒子所构成的晶体类型属分子晶体.
(5)c粒子是OH-,f粒子是H3O+(都用化学式表示).
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 单位电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
试写出:
(1)d分子的空间构型为三角锥形.
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:NaOH>Mg(OH)2 (用化学式表示).
(3)d溶于水的电离方程式NH3+H2O?NH3•H2O?NH4++OH-.
(4)g粒子所构成的晶体类型属分子晶体.
(5)c粒子是OH-,f粒子是H3O+(都用化学式表示).
9.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 1molCl2与1molFe反应,转移的电子数为3NA | |
| B. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA | |
| C. | 在标准状况下,Cl2和H2的混合气22.4升,光照后原子总数为2NA | |
| D. | 0.1mol•L-1的FeCl3溶液中含有0.1NA个Fe3+ |
16.下列离子方程式书写正确的是( )
| A. | 苯酚与碳酸钠反应:2C6H5OH+CO32-→2C6H5O-+CO2↑+H2O | |
| B. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| C. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O | |
| D. | SO2通入溴水中:SO2+2H2O+Br2═2H++SO42-+2HBr |
13.以乙醇为原料,合成乙二酸乙二酯(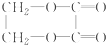 )所经历的反应的正确顺序是( )
)所经历的反应的正确顺序是( )
①氧化 ②消去 ③加成 ④酯化 ⑤水解 ⑥加聚.
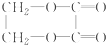 )所经历的反应的正确顺序是( )
)所经历的反应的正确顺序是( )①氧化 ②消去 ③加成 ④酯化 ⑤水解 ⑥加聚.
| A. | ①⑤②③④ | B. | ①②③⑤④ | C. | ②③⑤①④ | D. | ②③⑤①⑥ |
 (1)2003年夏,全球化学家投票评选了化学史上十项最美的实验,1848年巴斯德用手工在光学显微镜下把左型酒石酸盐晶体和右型酒石酸盐晶体分开的实验被选为十项之首.请回答下列问题:
(1)2003年夏,全球化学家投票评选了化学史上十项最美的实验,1848年巴斯德用手工在光学显微镜下把左型酒石酸盐晶体和右型酒石酸盐晶体分开的实验被选为十项之首.请回答下列问题: .
.