题目内容
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分。当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同)。右侧CO2与CO分子数之比为

A. 1:3 B. 3:1 C. 1:2 D. 2:1
【答案】A
【解析】
相同条件下,气体的体积之比等于其物质的量之比,1mol氮气占容器总体积的4/5,氮气和混合气体的体积之比为4:1,则其物质的量之比为4:1,所以混合气体的物质的量为0.25mol, 设一氧化碳的物质的量为x,二氧化碳的物质的量为y,则有关系式:x+y=0.25,28x+44y=8,解联立方程得,x= 0.1875、y=0.0625,CO2与CO的物质的量比为0.0625:0.1875=1:3,则CO2与CO分子数之比为1:3,故选A。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】实验室为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法不正确的是( )
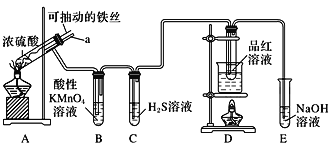
A.装置B中酸性KMnO4溶液逐渐褪色,体现了二氧化硫的还原性 |
B.实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的Fe3+ |
C.装置D中品红溶液褪色可以验证SO2的漂白性 |
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸 |