题目内容
【题目】某化学实验需要450 mL 0.10 mol·L-1 Na2CO3溶液,某同学选用Na2CO3·10H2O晶体进行配制,简要回答下列问题:
(1)该实验应选择__________mL容量瓶。
(2)需称取Na2CO3·10H2O的质量为__________g。
(3)该实验的正确操作顺序是_______________(填字母代号)。
A.用托盘天平称取Na2CO3·10H2O晶体
B.上下颠倒摇匀
C.用胶头滴管加水至刻度线
D.洗涤所用仪器并将洗涤液转移进容量瓶
E.将所称取的晶体溶于蒸馏水并冷却至室温
F.将溶液转入容量瓶
(4)另需配制一定浓度的NaOH溶液,称量时若将NaOH固体置于滤纸上称量,则所配溶液浓度______;若容量瓶中有检漏时残留的少量蒸馏水,会使所配溶液浓度______;NaOH溶解后未经______;立即注入容量瓶至刻度线,会使浓度______;定容时必须使凹液面最低处与刻度线相切,若仰视会使所配溶液浓度______(凡涉及浓度变化填“偏高”、“偏低”或“无影响”)。
(5)向200 mL所配的 0.10 mol·L-1Na2CO3溶液中逐滴加入10 mL 12.25%稀H2SO4(ρ=1.0 g/cm3),理论上能收集到标准状况下的气体__________mL。
【答案】500 14.3 A E F D C B 偏低 无影响 冷却 偏高 偏低 112
【解析】
(1)由于没有450mL容量瓶,则该实验应选择500mL容量瓶。
(2)需称取Na2CO3·10H2O的质量为0.5L×0.1mol/L×286g/mol=14.3g。
(3)配制一定物质的量浓度溶液的基本操作步骤是计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,则该实验的正确操作顺序是A、E、F、D、C、B。
(4)另需配制一定浓度的NaOH溶液,称量时若将NaOH固体置于滤纸上称量,由于氢氧化钠易吸水,则氢氧化钠的质量减少,因此所配溶液浓度偏低;若容量瓶中有检漏时残留的少量蒸馏水,由于不会影响溶质和溶液体积,则会使所配溶液浓度无影响;氢氧化钠溶于水放热,则NaOH溶解后未经冷却,立即注入容量瓶至刻度线,冷却后溶液体积减少,则会使浓度偏高;定容时必须使凹液面最低处与刻度线相切,若仰视会使溶液体积增加,所配溶液浓度偏低。
(5)200mL溶液中碳酸钠的物质的量是0.2L×0.1mol/L=0.02mol。10 mL 12.25%稀H2SO4(ρ=1.0 g/cm3)的物质的量是![]() ,其中氢离子的物质的量是0.025mol。由于与碳酸钠反应时分步进行,即首先转化为碳酸氢钠,消耗氢离子是0.02mol,剩余的氢离子再与碳酸氢钠反应放出二氧化碳,此时氢离子不足,则根据HCO3-+H+=CO2↑+H2O可知生成的二氧化碳是0.025mol-0.02mol=0.005mol,在标准状况下的体积是0.005mol×22.4L/mol=0.112L=112mL。
,其中氢离子的物质的量是0.025mol。由于与碳酸钠反应时分步进行,即首先转化为碳酸氢钠,消耗氢离子是0.02mol,剩余的氢离子再与碳酸氢钠反应放出二氧化碳,此时氢离子不足,则根据HCO3-+H+=CO2↑+H2O可知生成的二氧化碳是0.025mol-0.02mol=0.005mol,在标准状况下的体积是0.005mol×22.4L/mol=0.112L=112mL。

【题目】利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。
(1)T1℃时,在2L密闭容器中充入0.6molSO3,图1表示SO3物质的量随时间的变化曲线。

①平衡时,SO3的转化率为______(保留一位小数);在T1℃下反应2SO2(g)+O2(g) ![]() 2SO3(g) 的平衡常数为____________;若其他条件不变,在8min时压缩容器的体积至1L,则n(SO3)的变化曲线为_______(填字母)。
2SO3(g) 的平衡常数为____________;若其他条件不变,在8min时压缩容器的体积至1L,则n(SO3)的变化曲线为_______(填字母)。
②下表为不同温度(T)下反应2SO2(g)+O2(g) ![]() 2SO3(g) △H<0的化学平衡常数(K):
2SO3(g) △H<0的化学平衡常数(K):
T/℃ | T2 | T3 |
K | 20.5 | 4.68 |
由此推知,其他条件相同,在T1、T2、T3三种不同温度下,反应从开始至达到平衡时所需要的时间最长的是 _____________。(填“T1”、“T2”或“T3”)
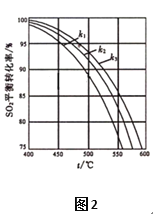
(2)在体系恒压的条件下进行反应:2SO2(g)+O2(g) ![]() 2SO3(g),原料气中SO2和O2的物质的量之比(k)不同时,SO2的平衡转化率与温度(t)的关系如图2所示:图中k1、k2、k3的大小顺序为____________。
2SO3(g),原料气中SO2和O2的物质的量之比(k)不同时,SO2的平衡转化率与温度(t)的关系如图2所示:图中k1、k2、k3的大小顺序为____________。