题目内容
下列说法错误的是
A.分子在化学反应中可以再分,原子在化学反应中不可再分
B.氧化性酸具有氧化性,还原性酸不具有氧化性
C.胶体、溶液、浊液均为混合物,电解质、非电解质均为化合物
D.12C、13C、14C为碳元素的三种核素,金刚石、石墨互为同素异形体
A.分子在化学反应中可以再分,原子在化学反应中不可再分
B.氧化性酸具有氧化性,还原性酸不具有氧化性
C.胶体、溶液、浊液均为混合物,电解质、非电解质均为化合物
D.12C、13C、14C为碳元素的三种核素,金刚石、石墨互为同素异形体
B
试题分析:A、分子是保持化学性质的一种微粒,而原子是化学变化中的最小微粒,因此分子在化学反应中可以再分,原子在化学反应中不可再分,A正确;B、氧化性酸是酸根表现出的,还原性酸中的氢元素具有氧化性,B不正确;C、胶体、溶液、浊液均为分散系,属于混合物,电解质、非电解质均为化合物,C正确;D、12C、13C、14C的质子数相同,中子数不同,为碳元素的三种核素,互为同位素。金刚石和石墨均是碳元素形成的单质,互为同素异形体,D正确,答案选B。

练习册系列答案
相关题目
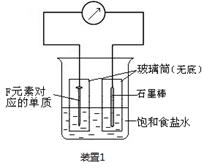
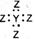
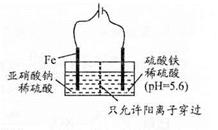
 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =" V" ( B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A ) _a( B )。
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =" V" ( B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A ) _a( B )。