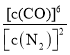题目内容
【题目】氮是一种重要的元素,可用来合成NH3与 HNO3等一系列重要化工产品。
(1)在标准状况下,1体积水溶解700体积氨气,所得溶液的密度为0.9g/mL,则该氨水的物质的量浓度是_______(小数点后保留一位)。
(2)合成氨的原料气N2和H2通常是以焦炭、水和空气为原料来制取的。其主要反应是:
①2C + O2 → 2CO ②C + H2O(g) → CO + H2 ③CO + H2O(g) → CO2 + H2
某次生产中将焦炭、H2O(g)和空气(设空气中N2和O2的体积比为4:1,下同)混合反应,所得气体产物经分析,组成如下表:
气体 | CO | N2 | CO2 | H2 | O2 |
体积(m3)(标准状况) | x | 20 | 12 | 60 | 1.0 |
则计算参加反应的H2O(g)和氧气的体积比V(H2O)/V(氧气)=__________上表中x=________m3,实际消耗了___________ kg焦炭。
(3)工业生产硝酸时尾气必须充分处理以避免环境污染,常用NaOH溶液吸收,吸收时发生反应:
①2NO2 + 2NaOH→NaNO3 + NaNO2 + H2O
②NO + NO2 + 2NaOH→2NaNO2 + H2O
现将22.4升(标准状况)NOx(只含NO、NO2,忽略其它成分)气体缓缓通入足量NaOH溶液中,充分反应,气体全部被吸收。则反应中产生NaNO3和NaNO2各多少克?(用含x的代数式表示)____________________
【答案】18.4 mol/L 15 44 30 85(x-1.5);69(2.5-x)
【解析】
(1)由标准状况下的体积可计算氨气的物质的量,利用氨气的质量和溶液的体积来计算物质的量浓度;
(2)N2的体积为20m3,空气中N2和O2的体积比为4:1,故O2的体积为5m3,故参加反应的O2的体积为5m3-1.0m3=4m3,根据方程式,结合表格数据进行计算,得出正确结论;
(3)NOx气体的物质的量为![]() =1mol,NO、NO2的平均组成为NOx,则NO与NO2的物质的量之比为
=1mol,NO、NO2的平均组成为NOx,则NO与NO2的物质的量之比为![]() ,设NO为amol,则NO2为(1-a)mol,则
,设NO为amol,则NO2为(1-a)mol,则![]() =
=![]() ,解得a=2-x,1-a=x-1,
,解得a=2-x,1-a=x-1,
根据方程式进行计算,得出正确结论。
(1)设水的体积为1L,氨气的体积为700L,则氨气的物质的量为![]() =31.25mol,
=31.25mol,
溶液的质量为1000g+31.25mol×17g/mol=1531.25g,
溶液的体积为![]() =1.7L,
=1.7L,
则氨水的物质的量浓度为c=![]() =18.4 mol/L;
=18.4 mol/L;
(2)N2的体积为20m3,空气中N2和O2的体积比为4:1,故O2的体积为![]() =5m3,故参加反应的O2的体积为5-1.0m3=4m3,
=5m3,故参加反应的O2的体积为5-1.0m3=4m3,
①2C+O2→2CO ②C+H2O(g)→CO+H2 ③CO+H2O(g)→CO2+H2
4 8 48 48 12 12 12
生成氢气的体积为12m3,故消耗的水的体积为60m3,则参加反应的H2O(g)和氧气的体积比V(H2O)/V(氧气)=![]() =15;
=15;
产物中二氧化碳的体积为12m3,故反应③生成氢气的体积为12m3,消耗CO的体积为12m3,
则反应②生成氢气的体积为60-12=48m3,故反应②生成CO的体积为48m3,消耗的C的物质的量为![]() ;
;
参加反应的O2的体积为4m3,故反应①生成CO的体积为8m3,消耗的C的物质的量为![]() ;
;
则所得气体产物中CO的体积为8m3+48m3-12m3=44m3,消耗的C的质量为=![]() ×12=30000g=30kg;
×12=30000g=30kg;
(3)NOx气体的物质的量为![]() =1mol,NO、NO2的平均组成为NOx,则NO与NO2的物质的量之比为
=1mol,NO、NO2的平均组成为NOx,则NO与NO2的物质的量之比为![]() ,
,
设NO为amol,则NO2为(1-a)mol,则![]() =
=![]() ,解得a=2-x,1-a=x-1,
,解得a=2-x,1-a=x-1,
①2NO2+2NaOH→NaNO3 +NaNO2 +H2O ②NO+NO2 +2NaOH→2NaNO2+H2O
2x-3 (x-1.5)(x-1.5)2-x 2-x 4-2x
反应②中反应的NO2的物质的量为(2-x)mol,则反应②中反应的NO2的物质的量为(2-x)mol,生成的NaNO2的物质的量为2×(2-x)=(4-2x)mol,
则反应①中反应的NO2的物质的量为x-1-(2-x)=(2x-3)mol,则反应①中生成的NaNO2的物质的量为![]() =(x-1.5)mol,生成的NaNO3的物质的量为(x-1.5)mol,
=(x-1.5)mol,生成的NaNO3的物质的量为(x-1.5)mol,
故反应中产生NaNO3的质量为85×(x-1.5)=(85x-127.5)g,
产生NaNO2的质量为69×(4-2x+x-1.5)=(172.5-69x)g,
答:产生NaNO3和NaNO2分别为(85x-127.5)g、(172.5-69x)g。

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】氯氨是氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl、NHCl2和NCl3),副产物少于其它水消毒剂。回答下列问题:
(1)①一氯胺(NH2Cl)的电子式为 ________________ 。
②工业上可利用反应Cl2(g)+NH3(g)=NH2Cl(g)+HCl(g)制备一氯胺,已知部分化学键的键能如下表所示(假设不同物质中同种化学键的键能相同),则该反应的△H=________。
化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
键能(kJ/mol) | 391 | 243 | 191 | 431 |
③一氯胺是重要的水消毒剂,其原因是由于一氯胺在中性、酸性环境中会发生水解,生成具有强烈杀菌消毒作用的物质,该反应的化学方程式为_________________________________。
(2)用Cl2和NH3反应制备二氯胺的方程式为2Cl2(g)+NH3(g)![]() NHCl2(l)+2HCl(g),向容积均为1 L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2 mol Cl2和2 mol NH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
NHCl2(l)+2HCl(g),向容积均为1 L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2 mol Cl2和2 mol NH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(Cl2)(甲容器)/mol | 2.00 | 1.50 | 1. 10 | 0.80 | 0.80 |
n(Cl2) (乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①甲容器中,0~40 min内用NH3的浓度变化表示的平均反应速率v(NH3)=___________。
②该反应的△H________0(填“>”或“<”) 。
③对该反应,下列说法正确的是______________(填选项字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.若容器内Cl2和NH3物质的量之比不变,则表明反应达到平衡状态
C.反应达到平衡后,其他条件不变,在原容器中充入一定量氦气,Cl2的转化率增大
D.反应达到平衡后,其他条件不变,加入一定量的NHCl2,平衡向逆反应方向移动
(3)在恒温条件下,2molCl2和1molNH3发生反应2Cl2(g)+NH3(g)![]() NHCl2(l)+2HCl(g),测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
NHCl2(l)+2HCl(g),测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
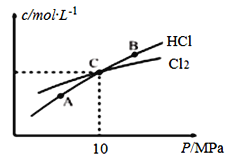
①A、B、C三点中Cl2转化率最高的是______点(填“A”“B”或“C”)。(提示:C点时HCl和Cl2的浓度相等)
②计算C点时该反应的压强平衡常数Kp(C)=_________(Kp是平衡分压代替平衡浓度计算,分压=总压×物质的量分数)