��Ŀ����
����Ŀ���ߴ����������Ϣ�����Ĺؼ����ϡ�
��1����Ԫ��λ�����ڱ���__________����_________�塣�����йع���ϵ�˵������ȷ����________(����ĸ)��
A.̼���軯ѧ�����ȶ�����������������ˮ��
B.������Ӳ�ȴ��۵�ߣ����������������մɺ����
C.�ߴ��ȵĶ���������������������ͨѶ���Ϲ��ά
D.��ͨ�������ɴ��ʯ��ʯ��ʯӢɰ�Ƴɵģ����ڲ�����ڵ�ȼH2ʱ���ֻ�ɫ����
E. ���������跴Ӧ���ʲ�������Ϊ��Һ�ⵥ����
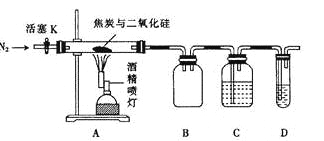
��2����ҵ����ʯӢɰ�ͽ�̿���Ƶôֹ衣
��֪��

�뽫���·�Ӧ���Ȼ�ѧ����ʽ����������SiO2(s)+2C(s)�TSi(s)+2CO(g) ��H=_____________
��3���ֹ辭ϵ�з�Ӧ�����ɹ���(SiH4)������ֽ����ɸߴ��裮��֪����ķֽ��¶�Զ���ڼ��飬��ԭ�ӽṹ������ԭ��________________________________��SiԪ�صķǽ���������CԪ�أ���������ȶ������ڼ��顣
��4�����ֹ�ת�����������(SiHCl3)����һ����ӦҲ���Ƶøߴ��衣
��SiHCl3�к��е�SiCl4��AsCl3�����ʶԾ�����������Ӱ�죮�����±����ݣ�����_________________�����ᴿSiHCl3��
���� | SiHCl3 | SiCl4 | AsCl3 |
�е�/�� | 32.0 | 57.5 | 131.6 |
����SiHCl3�Ʊ��ߴ���ķ�ӦΪSiHCl3(g)+H2(g) ![]() Si(s)+3HCl(g)����ͬ�¶��£�SiHCl3��ƽ��ת�����淴Ӧ���Ͷ�ϱȣ���Ӧ��ʼʱ������Ӧ������ʵ���֮�ȣ��ı仯��ϵ��ͼ��ʾ������˵����ȷ����_____________________������ĸ��ţ���
Si(s)+3HCl(g)����ͬ�¶��£�SiHCl3��ƽ��ת�����淴Ӧ���Ͷ�ϱȣ���Ӧ��ʼʱ������Ӧ������ʵ���֮�ȣ��ı仯��ϵ��ͼ��ʾ������˵����ȷ����_____________________������ĸ��ţ���
a.�÷�Ӧ��ƽ�ⳣ�����¶����߶�����
b.�������ʾ��Ͷ�ϱ�Ӧ����![]()
C.ʵ��������Ϊ���SiHCl3�������ʣ�Ӧ�ʵ������¶�
�������Ʊ����̱����ϸ������ˮ������SiHCl3��ˮ���ҷ�Ӧ����H2SiO3��HC1����һ�����ʣ�д����ƽ�Ļ�ѧ��Ӧ����ʽ��____________________________________��
���𰸡� 3 ��A BCD +638.4kJ��mol-1 C��Si������������ͬ������ͬ����Ԫ�ء����� Cԭ�Ӱ뾶С��Si����Cԭ�ӵ��Ӳ�������Si���� ������� a��c SiHCl3+3H2O===H2SiO3��+H2��+3HC1��
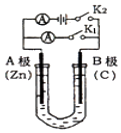
����������1����Ԫ���������Ӳ㣬�����4�����ӣ�λ�����ڱ��ĵ���������A�壻
A��̼��������ԭ�Ӿ��壬��ѧ�����ȶ����۵�ϸߣ�������������������ˮ�࣬��A����B���������մ����������ǽ�������֮һ��������Ӳ�ȴ��۵�ߣ����������������մɺ���У���B��ȷ��C�����ά�Ǹߴ��ȵĶ���������������������ͨѶ���ϣ���C��ȷ��D����ͨ�������ɴ��ʯ��ʯ��ʯӢɰ�Ƴɵģ�������Ԫ�أ��ڲ�����ڵ�ȼH2ʱ���ֻ�ɫ���棬��D��ȷ��E�������跴Ӧ���������ᷴӦ�����õ��������Ϊ��Һ�ⵥ���裬��E������
�ʴ�Ϊ��3����A��BCD��
��2������������Ӧ���������仯ͼ���֪��Si(s)+O2(s)=SiO2(s)��H=-859.4kJmol-1
2C(s)+O2(s)=2CO(g)��H=-221.0kJmol-1���õڶ�������ʽ��ȥ��һ������ʽ�ó����跴Ӧ��SiO2(s)+2C(s)=Si(s)+2CO(g)��H=+638.4 kJmol-1���õ���H=+638.4kJmol-1��
�ʴ�Ϊ��+638.4 kJmol-1��
��3������ķֽ��¶�Զ���ڼ��飬����ΪC��SiΪͬ����Ԫ�أ�������������ͬ��Cԭ�Ӱ뾶С��Si��SiԪ�صķǽ���������CԪ�أ����Թ�������ȶ������ڼ�����
�ʴ�Ϊ��C��Si������������ͬ������ͬ����Ԫ�ء�����Cԭ�Ӱ뾶С��Si����Cԭ�ӵ��Ӳ�������Si����
��4���ٸ��ݸ����ʷе�IJ�ͬ�����ᴿ���ʣ��������������
�ʴ�Ϊ���������
��a�������¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���÷�Ӧ��ƽ�ⳣ�����¶����߶�����a��ȷ��b������һ�ַ�Ӧ���Ũ�ȣ������������Ӧ���ת���ʣ���������ת���ʷ������ͣ��ʺ������ʾ��Ͷ�ϱ�Ӧ����![]() ����b����c�������¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���ʵ��������Ϊ���SiHCl3�������ʣ�Ӧ�ʵ������¶ȣ���c��ȷ���ʴ�Ϊ��ac��
����b����c�������¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���ʵ��������Ϊ���SiHCl3�������ʣ�Ӧ�ʵ������¶ȣ���c��ȷ���ʴ�Ϊ��ac��
��SiHCl3��H2O���ҷ�Ӧ����H2SiO3��HCl����һ�����ʣ��������ǻ��ϼ۵ı仯��֪��SiHCl3��H2SiO3+HCl������SiԪ�ػ��ϼ����ߣ� ClԪ�ػ��ϼ۲��䡣������ԭ��Ӧ���л��ϼ۵����ߣ����л��ϼ۵Ľ��ͣ���HԪ�صĻ��ϼ۱ض����ͣ���Ԫ��Ϊ-2�ۣ����ܽ���������һ��������H2��
�ʴ�Ϊ��SiHCl3+3H2O=H2SiO3��+H2��+3HCl����