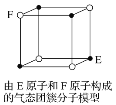
题目内容
【题目】下列说法正确的是( )
A.稀释Na2CO3溶液时,c(HCO3-)、![]() 均增大
均增大
B.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H<0,△S<0
C.用0.1molL-1CH3COOH溶液滴定0.1molL-1NaOH至中性时:c(CH3COO-)+c(CH3COOH)=c(Na+)
D.向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积减小
【答案】B
【解析】
A、稀释![]() 溶液时,碳酸根离子水解程度增大,生成的碳酸氢根物质的量增大,但是
溶液时,碳酸根离子水解程度增大,生成的碳酸氢根物质的量增大,但是![]() 变小;
变小;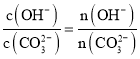 ,由于氢氧根离子物质的量增大,碳酸根的物质的量减少,比值增大,选项A错误;
,由于氢氧根离子物质的量增大,碳酸根的物质的量减少,比值增大,选项A错误;
B、该反应是自发进行的反应,常温下,反应![]() 的
的![]() ,
,![]() ,选项B正确;
,选项B正确;
C、滴定到溶液显示中性,醋酸的物质的量大于氢氧化钠的物质的量,溶液体积相同,![]() ,选项C错误;
,选项C错误;
D、温度没有变化,水的离子积没有变化,选项D错误;
答案选B。

【题目】Ⅰ.(1)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36。请用离子方程式说明上述除杂的原理__。
(2)在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则该温度下水的离子积常数KW=__。在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=___。
Ⅱ.工业生成尿素的原理是以NH3和CO2为原料合成尿素,反应的化学方程式为2NH3(g)+ CO2(g)![]() CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
(1)ΔH___0(填“>”、“<”或“=”)。
(2)在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)n(NH3)∶n(CO2)=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___。
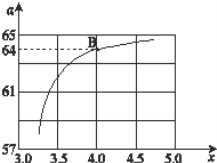
(3)图中的B点对应的NH3的平衡转化率为__。