题目内容
20.氰气[(CN)2]和氰化物都是剧毒性物质,氰分子的结构式为N≡C-C≡N,性质与卤素相似,下列叙述错误的是( )| A. | 氰分子中四原子共直线 | |
| B. | 氰分子中C≡N键长大于C≡C键长 | |
| C. | 氰气分子中含有σ键和π键 | |
| D. | 氰化氢在一定条件下能与烯烃发生加成反应 |
分析 A.直接连接三键两端原子的原子与三键两端的原子共线,正负电荷重心重合的分子为非极性分子;
B.同一周期元素中,原子半径随着原子序数的增大而减小,原子半径越大其键长越长;
C.共价单键是σ键,共价双键中一个是σ键一个是π键,共价三键中一个是σ键两个是π键;
D.根据卤素单质的性质分析氰化氢的性质.
解答 解:A.直接连接三键两端原子的原子与三键两端的原子共线,正负电荷重心重合的分子为非极性分子,该反应中所有原子共线,且该分子的正负电荷重心重合,为非极性分子,故A正确;
B.同一周期元素中,原子半径随着原子序数的增大而减小,原子半径越大其键长越长,碳原子半径大于氮原子,所以氰分子中C≡N键长小于C≡C键长,故B错误;
C.共价单键是σ键,共价双键中一个是σ键一个是π键,共价三键中一个是σ键两个是π键,所以氰气分子中含有3个σ键和4个π键,故C正确;
D.根据卤素性质知,卤素单质能和乙烯发生加成反应,则氰分子在一定条件下能与烯烃发生加成反应,故D正确;
故选B.
点评 本题考查了物质的组成、结构和性质的关系,同时考查学生知识迁移能力,根据已知的乙炔的结构、卤素的性质结合元素周期律来分析解答即可,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
10.在反应2SO2+18O2?2SO3中,其中氧气用18O标记上,其中含有18O的物质有( )
| A. | SO2 | B. | O2 SO3 | C. | SO2 O2 SO3 | D. | SO2 SO3 |
11.元素周期表中某区域可以寻找制备新型农药材料的元素,它们是( )
| A. | 左下方区域的金属元素 | |
| B. | 右上方区域的某些非金属元素 | |
| C. | 金属元素和非金属元素分界线附近的元素 | |
| D. | 过渡元素区域 |
5.下列四个原电池的有关说法正确的是( )
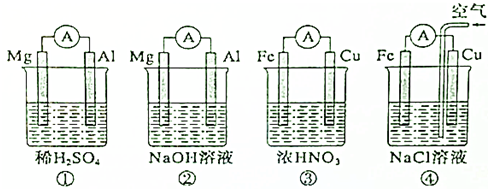

| A. | 装置①中SO42-的向Al片移动 | |
| B. | 装置②中的Mg片上发生的反应为:2H++2e-═H2↑ | |
| C. | 装置③中铁片被氧化,铜片上产生气体 | |
| D. | 装置④中若有1摩尔铁锈(氧化铁)生成,理论上有4摩尔电子通过导线 |
9. 鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )
鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )
 鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )
鸦片最早用于药物(有止痛、止泻、止渴作用),长期服用会成瘾,使人体质衰弱、精神颓废、寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如图所示:已知该物质的燃烧产物为CO2、H2O和N2,1mol该化和物完全燃烧的耗氧量及在一定条件下与H2发生加成反应的耗氢量分别为( )| A. | 26.5mol 8mol | B. | 23.25mol 8mol | C. | 23.25mol 10mol | D. | 26.5mol 6mol |
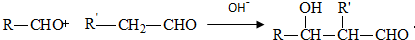 .有机物G(C20H18O4)是一种酯,合成路线如下:
.有机物G(C20H18O4)是一种酯,合成路线如下:
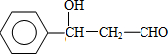 ;F的结构简式:CH2OHCH2OH;
;F的结构简式:CH2OHCH2OH; .
.