题目内容
17.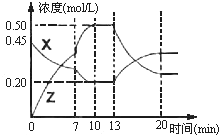 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )| A. | 化学方程式中a:b=1:3 | |
| B. | 推测在第7min时曲线变化的原因可能是升温 | |
| C. | 推测在第13min时该反应刚好达到化学平衡 | |
| D. | 用X表示O~10min内该反应的平均速率为v(X)=0.045mol•L-1•mol-1 |
分析 A.根据物质的量变化量之比等于化学计量数之比计算;
B.第7min时,单位时间内X、Z的物质的量变化量较大,反应速率增大;
C.据第13min时的图象变化分析;
D.根据v=$\frac{△c}{△t}$计算反应速率.
解答 解:A、物质的量变化量之比等于化学计量数之比,方程式中a:b=(0.45-0.2):(0.50-0)=1:2,故A错误;
B、第7min时,单位时间内X、Z的物质的量变化量较大,反应速率增大,可能为升高温度,故B正确;
C、第13min时,Z的物质的量减小,X的物质的量增大,平衡影响正反应方向移动,没有达到平衡状态,故C错误;
D、0~10min内v(X)=$\frac{\frac{0.45mol-0.2mol}{1L}}{10min}$=0.025mol/(L•min),故D错误;
故选B.
点评 本题考查化学平衡以及反应速率等问题,题目难度中等,注意图象曲线变化的分析,把握外界条件对平衡移动的影响.

练习册系列答案
相关题目
7.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝溶液中加入过量氨水Al3++4NH3 H2O=AlO2-+4NH4++2H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| C. | 碳酸钙溶于醋酸 CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气 2Fe2++Cl2=2Fe3++2Cl- |
5.用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能还有杂质气体( )
①CO2 ②HCl ③H2O ④O2.
①CO2 ②HCl ③H2O ④O2.
| A. | ①②③④ | B. | ②③④ | C. | ②③ | D. | ①④ |
2.质量数为27的元素R,其核内有14个中子,则R可形成的离子为( )
| A. | R+ | B. | R2+ | C. | R3+ | D. | R2- |
9.下列不属于基本反应类型的是( )
| A. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+2CO2 | B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | ||
| C. | NaHCO3+NaHSO4═Na2SO4+CO2↑+H2O | D. | 2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑ |
7.下列说法中正确的是( )
| A. | 在50mL量筒中配制0.1000mo1•L-1碳酸钠溶液 | |
| B. | 0.5mol O3与11.2L O3所含的分子数一定相等 | |
| C. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| D. | 常温常压下,22.4L的NO2和CO2混合气体含有2NA的氧原子 |