题目内容
7.下列反应的离子方程式书写正确的是( )| A. | 氯化铝溶液中加入过量氨水Al3++4NH3 H2O=AlO2-+4NH4++2H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| C. | 碳酸钙溶于醋酸 CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气 2Fe2++Cl2=2Fe3++2Cl- |
分析 A.反应生成氢氧化铝、氯化铵;
B.少量小苏打完全反应,生成碳酸钙、水、NaOH;
C.醋酸在离子反应中保留化学式;
D.反应生成氯化铁,遵循电子、电荷守恒.
解答 解:A.氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3 H2O=Al(OH)3↓+3NH4+,故A错误;
B.澄清石灰水与少量小苏打溶液混合的离子反应为Ca2++OH-+HCO3-=CaCO3↓+H2O,故B正确;
C.碳酸钙溶于醋酸的离子反应为CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O,故C错误;
D.氯化亚铁溶液中通入氯气的离子反应为2Fe2++Cl2=2Fe3++2Cl-,故D正确;
故选BD.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
18.下列试剂不能用于除去H2中混有的CO2杂质的是( )
| A. | NaOH溶液 | B. | Na2CO3溶液 | C. | Ba(OH)2溶液 | D. | H2SO4溶液 |
2.下列各组溶液,不用其他试剂就可以将它们区别开的是( )
| A. | HCl、K2CO3、KOH、K2SO4 | B. | NaNO3、HCl、NH4Cl、KOH | ||
| C. | BaCl2、CaCl2、Na2SO4、KNO3 | D. | K2CO3、KOH、MgSO4、KHSO4 |
19.下列各组中的元素,同属于第3周期的是( )
| A. | 氧、碳、氮 | B. | 钠、铝、硅 | C. | 镁、铝、氧 | D. | 氯、溴、碘 |
16.能正确表示下列反应的离子方程式的是( )
| A. | 向Fe(NO3)2溶液中加稀盐酸:3Fe2++NO3-+4H+=3Fe2++NO↑+2H20 | |
| B. | 硫化钠溶于过量稀硝酸中:S2-+2H+═H2S↑ | |
| C. | 过量CO2通入氢氧化钠溶液中:2OH-+CO2═CO32-+H20 | |
| D. | 大理石溶于醋酸中:CaCO3+2H+═Ca2++CO2↑+H20 |
17.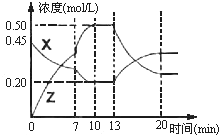 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )| A. | 化学方程式中a:b=1:3 | |
| B. | 推测在第7min时曲线变化的原因可能是升温 | |
| C. | 推测在第13min时该反应刚好达到化学平衡 | |
| D. | 用X表示O~10min内该反应的平均速率为v(X)=0.045mol•L-1•mol-1 |