题目内容
5.用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能还有杂质气体( )①CO2 ②HCl ③H2O ④O2.
| A. | ①②③④ | B. | ②③④ | C. | ②③ | D. | ①④ |
分析 浓盐酸易挥发,次氯酸钙能够与空气中的二氧化碳、水反应生成碳酸钙和次氯酸,次氯酸分解生成氯化氢和氧气,盐酸与碳酸钙反应生成二氧化碳气体,据此解答.
解答 解:次氯酸钙能够与空气中的二氧化碳、水反应生成碳酸钙和次氯酸,次氯酸分解生成氯化氢和氧气,贮存很久的漂白粉可能存在碳酸钙,贮存很久的漂白粉可能存在碳酸钙,加盐酸发生Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O、CaCO3+2HCl=CaCl2+CO2↑+H2O,
浓盐酸易挥发,从溶液中生成的气体中会混有水蒸气,则制得的氯气中,可能含有杂质气体为CO2、HCl、H2O(气)、O2,
故选:A.
点评 本题考查了元素化合物知识,熟悉次氯酸钙、次氯酸的性质是解题关键,题目难度不大.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
16.能正确表示下列反应的离子方程式的是( )
| A. | 向Fe(NO3)2溶液中加稀盐酸:3Fe2++NO3-+4H+=3Fe2++NO↑+2H20 | |
| B. | 硫化钠溶于过量稀硝酸中:S2-+2H+═H2S↑ | |
| C. | 过量CO2通入氢氧化钠溶液中:2OH-+CO2═CO32-+H20 | |
| D. | 大理石溶于醋酸中:CaCO3+2H+═Ca2++CO2↑+H20 |
13.某物质在一定条件下按下式分解:2A═B↑+2C↑+2D↑,测得生成的混合气体在相同条件下密度是H2密度d倍,则A的式量为( )
| A. | 2d | B. | 2.5d | C. | 5d | D. | 10d |
17.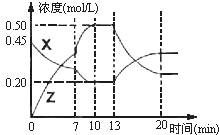 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )| A. | 化学方程式中a:b=1:3 | |
| B. | 推测在第7min时曲线变化的原因可能是升温 | |
| C. | 推测在第13min时该反应刚好达到化学平衡 | |
| D. | 用X表示O~10min内该反应的平均速率为v(X)=0.045mol•L-1•mol-1 |
14.1mol H2和32g O2的体积,前者与后者的关系是( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能确定 |
 室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示.
室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示.