题目内容
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
| A.AlON和石英的化学键类型相同 |
| B.AlON和石英晶体类型相同 |
| C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
D
解析试题分析:A、氮氧化铝和石英都是原子晶体,化学键类型相同,正确;B、二者都是原子晶体,正确;C、氮氧化铝含有共价键而氧化铝含有离子键,化学键的类型不同,正确;D、氧化铝是离子晶体,二者类型不同,错误。
考点:考查了化合物的成键类型。

练习册系列答案
相关题目
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)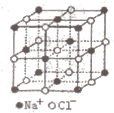
| A.一个金刚石的晶胞中有8个C原子 |
| B.金刚石的密度为3.54g·cm-1 |
| C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D.在该种CO2晶胞中含氧原子8个 |
最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是
| A.该晶体类型是原子晶体 |
| B.晶体中碳原子数与C—O化学键数之比为1∶2 |
| C.晶体的空间最小环共有12个原子构成 |
| D.该晶体中碳原子和氧原子的个数比为1∶2 |
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位。小黑球表示阳离子,小白球表示阴离子,该离子化合物中,阴、阳离子个数比是
| A.1∶8 | B.1∶4 | C.1∶2 | D.1∶1 |
原子晶体干冰具有类似SiO2的晶体结构,下列有关它的推断中,错误的是
| A.它可作耐磨材料 |
| B.它不可用作致冷剂 |
| C.晶体中每个碳原子形成2个碳氧双键 |
| D.晶体中碳、氧原子个数之比为1:2 |
据美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800 K,制得具有高熔点、高硬度的二氧化碳晶体。下列关于该晶体的说法正确的是( )
| A.该晶体属于分子晶体 |
| B.该晶体易汽化,可用作制冷材料 |
| C.一定条件下,该晶体可跟氢氧化钠反应 |
| D.每摩尔该晶体中含5 mol C—O键 |
关于金属晶体的体心立方密堆积的结构型式的叙述中,正确的是( )。
| A.晶胞是六棱柱 |
| B.属于A2型密堆积 |
| C.每个晶胞中含有4个原子 |
| D.每个晶胞中含有5个原子 |
下列叙述不正确的是( )
| A.金刚石、碳化硅、晶体硅的熔点依次降低 |
| B.CaO晶体结构与NaCl晶体结构相似,每个CaO晶胞中含有4个Ca2+和4个O2- |
C.设NaCl的摩尔质量为M g·mol-1,NaCl的密度为ρ g·cm-3,阿伏加德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为 · · cm cm |
| D.X、Y可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角位置,则该晶体的组成式为XY3 |
