题目内容
关于金属晶体的体心立方密堆积的结构型式的叙述中,正确的是( )。
| A.晶胞是六棱柱 |
| B.属于A2型密堆积 |
| C.每个晶胞中含有4个原子 |
| D.每个晶胞中含有5个原子 |
B
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
科学家最近又发现了一种新能源——“可燃冰”。它的主要成分是甲烷分子的结晶水合物(CH4·nH2O)。其形成过程是:埋于海底地层深处的大量有机质在缺氧环境中,厌氧型细菌把有机质分解,最后形成石油和天然气,其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”。这种“可燃冰”的晶体类型是( )
| A.离子晶体 | B.分子晶体 | C.原子晶体 | D.金属晶体 |
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
| A.AlON和石英的化学键类型相同 |
| B.AlON和石英晶体类型相同 |
| C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
下列说法正确的是
| A.Mg2+的半径小于N3-的半径 |
| B.H2O比H2S稳定是因为H2O中存在分子间氢键 |
| C.SiO2因的相对分子质量大于CO2,所以SiO2的熔点高于CO2 |
| D.由原子构成的晶体一定是原子晶体 |
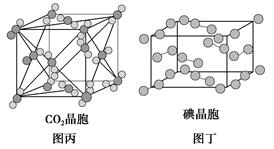
有关晶体的结构如图所示,下列说法中不正确的是( )。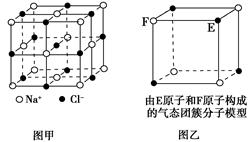
| A.在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体 |
| B.该气态团簇分子(图乙)的分子式为EF或FE |
| C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻 |
| D.在碘晶体(图丁)中,碘分子的排列有两种不同的方向 |
下列性质适合于分子晶体的是( )。
| A.熔点1 070 ℃,易溶于水,水溶液能导电 |
| B.熔点10.31 ℃,液态不导电,水溶液导电 |
| C.难溶于CS2,熔点1 128 ℃,沸点4 446 ℃ |
| D.熔点97.81 ℃,质软导电,密度0.97 g·cm-3 |
水的状态除了气、液、固态外还有玻璃态。它是由液态水急速冷却到165 K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )。
| A.水由液态变为玻璃态,体积缩小 |
| B.水由液态变为玻璃态,体积膨胀 |
| C.玻璃态是水的一种特殊状态 |
| D.玻璃态水是分子晶体 |
氮化硅是一种新合成的超硬、耐磨、耐高温的材料。下列对氮化硅的叙述中,正确的是( )。
| A.氮化硅是分子晶体 |
| B.氮化硅是原子晶体 |
| C.氮化硅是离子晶体 |
| D.氮化硅化学式为Si4N3 |
关于晶体的自范性,下列叙述正确的是( )。
| A.破损的晶体能够在固态时自动变成规则的多面体 |
| B.缺角的氯化钠晶体在饱和的NaCl溶液中慢慢变为完美的立方块 |
| C.圆形容器中结出的冰是圆形的 |
| D.由玻璃制成的圆形的玻璃球 |