题目内容
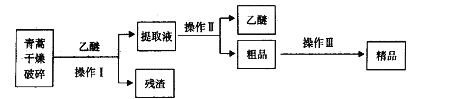
【题目】硝酸铝[Al(NO3)3]是一种常用媒染剂。工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)39H2O]的流程如图甲:
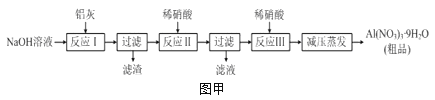
(1)写出反应Ⅰ的离子方程式:______________________________________________。
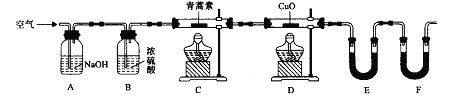
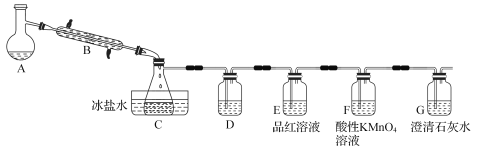
(2)若用图乙所示实验装置制取Al(NO3)3,通入水蒸气的作用是__________________。
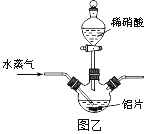
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的是__________。
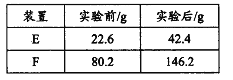
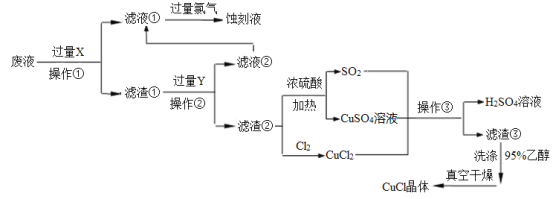
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和某气体。已知:2NO2+2NaOH=NaNO2+NaNO3。为了确定生成气体的成分,某学生拟用下列装置进行实验。
①进行实验时装置接口正确顺序是A→________________________→F。
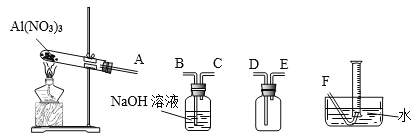
②证明分解生成的混合气体中有NO2的现象是_____________________。
③取21.3g Al(NO3)3加热分解,用排水法收集气体,最终在标准状况下收集到_____mL气体,结合化学方程式说明理由____________________________。
(5)设计实验证明粗品中含有Al(NO3)3:_________________________。
【答案】
(1)2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑、Al2O3+2OH﹣=2AlO2﹣+H2O(2分)
(2)提高温度、搅拌,加快反应速率(1分)
(3)抑制硝酸铝水解(1分)
(4)①E→D→B→C(2分)
②加热后大试管、安全瓶中出现棕红色气体,通过NaOH溶液的洗气瓶后棕红色气体消失(2分)
③0(1分)
因为4Al(NO3)32Al2O3+12NO2↑+3O2↑;4NO2↑+O2↑+2H2O=4HNO3,故收集不到气体(2分)
(5)取少量粗品于试管中加水溶解,再向试管中滴加NaOH溶液,先产生白色沉淀,后沉淀又溶解,证明含有Al3+;另取少量粗品于试管中,向试管中加入70%的H2SO4,再加入铜片,在试管上方产生棕红色气体,说明含有NO3-。(或加热粗品,有红棕色气体产生,说明含有NO3-)(3分)
【解析】
试题分析:流程是铝灰用氢氧化钠溶液溶解,铝、氧化铝反应生成偏铝酸钠,氧化铁不反应,过滤分离,滤液中含有偏铝酸钠、未反应的NaOH,加入硝酸中和未反应的氢氧化钠,并将偏铝酸钠转化为氢氧化铝沉淀,再过滤分离,氢氧化铝沉淀再用硝酸溶解,得到硝酸铝溶液,经过减压蒸发得到硝酸铝晶体。
(1)反应Ⅰ涉及:铝与氢氧化钠反应生成偏铝酸钠与氢气,氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应方程式为:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑、Al2O3+2OH﹣=2AlO2﹣+H2O;
(2)由于水蒸气温度较高,可以升高反应体系的温度,且可以起搅拌作用,可以加快反应速率;
(3)硝酸铝容易发生水解,减压蒸发、反应Ⅲ中加入的稀硝酸稍过量,都可以抑制硝酸铝水解;
(4)①因为NO2易溶于水,大试管应先防倒吸接E→D,再吸收NO2接B→C;
②加热生成NO2,故大试管、安全瓶中出现棕红色气体,通过NaOH溶液的洗气瓶后棕红色气体消失。
③因为4Al(NO3)32Al2O3+12NO2↑+3O2↑;4NO2↑+O2↑+2H2O=4HNO3,故收集不到气体。
(5)取少量粗品于试管中加水溶解,再向试管中滴加NaOH溶液,先产生白色沉淀,后沉淀又溶解,证明含有Al3+;另取少量粗品于试管中,向试管中加入70%的H2SO4,再加入铜片,在试管上方产生棕红色气体,说明含有NO3-。(或加热粗品,有红棕色气体产生,说明含有NO3-)。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | ||||||||||||||||
c | d | e | |||||||||||||||
f | g | ||||||||||||||||
试回答下列问题(凡涉及的物质均用化学式表示):
(1)a的氢化物的分子构型为 ,中心原子的杂化形式为 ;d的最高价氧化物的分子构型为 ,中心原子的杂化形式为 ,该分子是 (填“极性”或“非极性”)分子。
(2)b、d、e三种元素的氢化物中的沸点最高的是 ,原因是: 。
(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式(必须将配位键表示出来) 。
(4)f(NH3)5BrSO4可形成两种配合物 ,已知f3+ 的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为 ,该配合物的配体是 、 ;