题目内容
【题目】(1)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1.K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1.K2的值如下表:
700 ℃ | 900 ℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
①反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=_________________(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)
CO(g)+H2O(g) ΔH的平衡常数为K,则ΔH=_________________(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)![]() CO(g)+H2O(g)是___________________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是___________________反应(填“吸热”或“放热”)。
②能判断CO2(g)+H2(g)![]() CO(g)+H2O(g)达到化学平衡状态的依据是_______(填字母)。
CO(g)+H2O(g)达到化学平衡状态的依据是_______(填字母)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
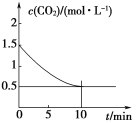
①用CO表示的化学反应速率为_________________________,该反应平衡常数的表达式为______________________________,该条件下反应的平衡常数为______;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为______mol·L-1。
②下列措施中能使平衡时![]() 增大的是________(填字母)。
增大的是________(填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
【答案】△H1-△H2K1/K2吸热BC0.1mol·L-1·min-1k=[CO]/[CO2]2.01.33A
【解析】
(1)①据已知热化学方程式,利用盖斯定律解答;据化学平衡常数表达式分析;
②根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(2)①依据平衡常数概念写出,用生成物平衡浓度幂次方乘积除以反应物平衡浓度的幂次方乘积得到平衡常数表达式,代入图上数据即可求K;据K求算二氧化碳的平衡浓度;
②c(CO)/c(CO2)是该反应的平衡常数表达式,平衡常数随温度变化,结合平衡移动原理分析判断.
(1)①已知①反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1;②反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;②反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2;据盖斯定律,①-②得:CO2(g)+H2(g)
FeO(s)+H2(g) ΔH2,平衡常数为K2;据盖斯定律,①-②得:CO2(g)+H2(g)![]() CO(g)+H2O(g)△H=△H1-△H2;反应的K=[CO]·[H2O]/[CO2]·[H2],K1=[CO]/[CO2],K2=[H2]/[H2O],所以K=K1/K2;K1随温度的升高而增大,K2随温度升高而减小,则K随温度升高而增大,说明正反应吸热;
CO(g)+H2O(g)△H=△H1-△H2;反应的K=[CO]·[H2O]/[CO2]·[H2],K1=[CO]/[CO2],K2=[H2]/[H2O],所以K=K1/K2;K1随温度的升高而增大,K2随温度升高而减小,则K随温度升高而增大,说明正反应吸热;
②A、反应前后气体体积不变,容器中压强始终不变,故A错误;
B、CO浓度不变,说明各气体浓度都不再变化,反应达到平衡状态,故B正确;
C、v正(H2)=v正(H2O)=v逆(H2O),正逆反应速率相等,但不为0,故C正确;
D、c(CO2)=c(CO)可能是平衡状态,也可能不是,与各物质的初始浓度及转化率有关,故D错误;
故选BC;
(2)①用CO表示的化学反应速率为v(CO)=v(CO2)=(1.5-0.5)mol·L-1/10min=0.1mol·L-1·min-1,该反应平衡常数的表达式为k=[CO]/[CO2]; 据图分析平衡时二氧化碳和CO的浓度分别为0.5mol·L-1和1mol·L-1,K=[CO]/[CO2]=1.0mol·L-1/0.5mol·L-1=2.0;若CO2的起始浓度为2.0mol·L-1,据方程式可知,反应的二氧化碳的浓度与生成CO浓度相等,设为xmol·L-1,则平衡时二氧化碳浓度为(2.0-x)mol·L-1,K=[CO/[CO2]=x/(2.0-x)=2.0,x=4/3=1.33;
②平衡常数随温度变化,不随浓度压强等因素变化,反应是吸热反应,升温平衡时K增大;
A.升高温度,平衡正向进行,平衡常数增大,故A正确;
B.增大压强,平衡不动,平衡常数不变,故B错误;
C.充入一定量CO2,平衡正向进行,但平衡常数不变,故C错误;
D.再加入一定量铁粉,平衡不移动,平衡常数不变,故D错误;
故选A.

【题目】合成氨工业中氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g) ![]() CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如下表所示:
CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如下表所示:
化学键 | C—H | O—H | C=O | H—H |
吸收热量(kJ/mol) | 414 | 464 | 803 | 436 |
试通过计算判断,下列有关甲烷转化成氢气过程的能量变化示意图正确的是
A. 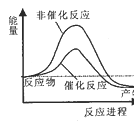 B.
B.  C. C
C. C D.
D.