题目内容
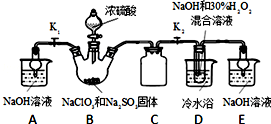
17.高铁酸钾(K2FeO4)是一种集氧化、吸附、速凝于一体的新型多功能水处理剂.其生产流程如下:
(1)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度是10mol/L.
(2)在溶液I中加入KOH固体的目的是AC(填编号).
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使副产物KClO3转化为 KClO
(3)每制得59.4克K2FeO4,理论上消耗氧化剂的物质的量为0.45 mol.从溶液II中分离出K2FeO4后,还得到副产品KNO3、KCl,写出③中反应的离子方程式:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
(4)高铁酸钾(K2FeO4)溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是4FeO42-+20 H+=4Fe3++3O2↑+10H2O.
分析 氢氧化钾溶液中充入足量氯气,在温度较低的条件下反应生成氯化钾、次氯酸钾和水,加入氢氧化钾固体除去KCl,得到碱性KClO的浓溶液,加入90%硝酸铁溶液发生反应生成高铁酸钾溶液Ⅱ纯化得到湿产品,洗涤干燥得到K2FeO4晶体;
(1)根据n=$\frac{m}{M}$计算出氢氧化钾的物质的量,溶液质量等于溶质质量与溶剂质量之和,利用V=$\frac{m}{ρ}$计算溶液体积,再根据c=$\frac{n}{V}$计算氢氧化钾溶液的物质的量浓度;
(2)根据生产工艺流程图,第①步氯气过量,第③步需要碱性条件,在温度较高时KOH 与Cl2 反应生成的是KClO3,氧化还原反应中化合价有升有降;
(3)反应③是次氯酸根离子在碱溶液中氧化铁离子为高铁酸根离子,根据题目信息、氧化还原反应中化合价发生变化确定产物以及电子得失守恒和质量守恒来配平;
(4)向高铁酸钾溶液中滴加稀硫酸,溶液变黄色,说明生成Fe3+,并产生大量气泡,应为氧气,说明高铁酸钾在酸性条件下自身发生氧化还原反应,生成铁离子、氧气和水,以此解答.
解答 解:(1)61.6g KOH固体的物质的量为$\frac{61.6g}{56g/mol}$=1.1mol,溶液的质量为100mL×1g/mL+61.6g=161.6g,所以溶液的体积为$\frac{161.6g}{1.47×1{0}^{-3}g/L}$=$\frac{161.6}{1470}$L,所以氢氧化钾溶液的物质的量浓度为$\frac{1.1mol}{\frac{161.6}{1470}L}$=10mol/L,
故答案为:10;
(2)由工艺流程可知,反应液I中有过量的Cl2反应,加KOH固体的目的是与过量的Cl2继续反应,生成更多的KClO.
A、与过量的Cl2继续反应,生成更多的KClO,故A正确;
B、由信息②可知温度较高KOH与Cl2 反应生成的是KClO3,不利用KClO生成、浪费原料,故B错误;
C、由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,故C正确;
D、由信息可知,该条件下KClO3 不能转化为KClO,故D错误.
故选:AC;
(3)据题目信息和氧化还原反应中化合价发生变化确定找出反应物:Fe3+、ClO-,生成物:FeO42-、Cl-,根据电子得失守恒和质量守恒来配平,可得③中反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
每制得59.4克K2FeO4,物质的量=$\frac{59.4g}{198g/mol}$=0.3mol,理论上消耗氧化剂为KClO的物质的量 依据离子方程式定量关系计算,
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
3 2
n 0.3mol
n=0.45mol
故答案为:0.45,2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(4)向高铁酸钾溶液中滴加稀硫酸,溶液变黄色,说明生成Fe3+,并产生大量气泡,应为氧气,反应的离子方程式为4FeO42-+20 H+=4Fe3++3O2↑+10H2O,说明高铁酸钾在酸性条件下自身发生氧化还原反应,
故答案为:4FeO42-+20 H+=4Fe3++3O2↑+10H2O.
点评 本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,培养了学生运用知识的能力.本题考查了物质制备与物质分离提纯的分析判断,实验过程的理解应用和基本操作的分析应用,掌握基础是关键,题目难度中等.

 精英口算卡系列答案
精英口算卡系列答案| A. | Cu(OH)2与盐酸 Cu(OH)2与醋酸 | |
| B. | BaCl2溶液与Na2SO4溶液 Ba(OH)2溶液与Na2SO4溶液 | |
| C. | NaHCO3溶液与NaHSO4溶液 Na2CO3溶液与NaHSO4溶液 | |
| D. | 石灰石与硝酸 生石灰与盐酸 |
| A. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5mol | |
| B. | 6.4gS6与S8的混合物中所含S原子数一定为0.4NA | |
| C. | 标准状况下,22.4L苯中含NA个分子 | |
| D. | 1molH2SO4中所含的粒子数目一定是NA |