题目内容
2.对二甲苯(PX)是生产矿泉水瓶(聚对苯二甲酸乙二醇酯,简称PET)的必要原料,生产涉及的反应之一如图所示.下列有关说法错误的是( )
| A. | PX分子中既含σ键又含π键 | |
| B. | PTA是该反应的氧化产物 | |
| C. | PTA与乙二醇通过加聚反应即可生产PET塑料 | |
| D. | 该反应每消耗1molPX,共转移12NA个电子(NA为阿伏伽德罗常数) |
分析 A.苯环中含有π键,C-H键中含有σ键;
B.反应中Mn元素的化合价降低,作氧化剂,则PX作还原剂;
C.对二甲苯与乙二醇发生缩聚反应;
D.根据Mn元素的化合价判断.
解答 解:A.苯环中含有π键,C-H键中含有σ键,所以PX分子中既含σ键又含π键,故A正确;
B.反应中Mn元素的化合价降低,作氧化剂,则PX作还原剂,所以PTA是该反应的氧化产物,故B正确;
C.PTA与乙二醇通过缩聚反应即可生产PET塑料,对二甲苯与乙二醇之间不能发生加聚反应,故C错误;
D. 反应中,Mn元素的化合价从+7价降低到+2价,转移5个电子,则1molPX反应消耗$\frac{12}{5}$molMnO4-,共转移12NA个电子,故D正确.
反应中,Mn元素的化合价从+7价降低到+2价,转移5个电子,则1molPX反应消耗$\frac{12}{5}$molMnO4-,共转移12NA个电子,故D正确.
故选C.
点评 本题考查了共价键的类型、有机反应类型、氧化还原反应等,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12.下列关于该温度下的叙述正确的是( )
| A. | 向氯化银的悬浊液中加入氯化钠溶液,Ksp(AgCl)减小 | |
| B. | 饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 | |
| C. | 若向0.0008mol•L-1的K2CrO4溶液中加入等体积0.002 mol•L-1的AgNO3溶液,则CrO42--完全沉淀 | |
| D. | 若将0.001mol•L-1AgNO3溶液滴入浓度均为0.001 mol•L-1的KCl和K2CrO4混合溶液中,则先产生AgCl沉淀 |
7. O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下:
O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下:
反应Ⅰ:O3+2I-+2H+=I2+O2+H2O
(1)用双线桥标示反应Ⅰ的电子转移情况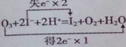 .
.
(2)I2可以继续与I-发生反应Ⅱ:I2(aq)+I-(aq)?I3-(aq)△H,为探究外在条件对I3-生成速率的影响,做了如下三组实验,完成表中的内容(表中不要留空格):
(3)用离子色谱仪测定I3-浓度随时间变化如图所示:
①反应Ⅱ的△H<0(填“>”“<”或“=”)
②实验B 10s内,I3-的生成速率为8.8×10-4mol/(L.s).
③实验B 18s后,I3-生成速率降低的主要原因是I-浓度降低.
(4)为进一步探究FeCl2对I3-生成速率的影响,提出合理假设,
假设一:Fe2+对反应起催化作用;
假设二:Cl-对反应起催化作用.
(5)请你设计实验验证上述假设一,写出实验步骤及结论.
实验步骤及结论:取一定量NaI溶液,加入稀硫酸调节pH=5.2,将溶液均分为两份A和B,向A、B试管中分解加入等物质的量的FeSO4、Na2SO4固体少许,之后同时向两支试管中通入O3,用离子色谱仪测定10s后I3-浓度,若cA(I3-)>cB(I3-),说明假设一成立,若cA(I3-)=cB(I3-),则假设一不成立.
 O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下:
O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下:反应Ⅰ:O3+2I-+2H+=I2+O2+H2O
(1)用双线桥标示反应Ⅰ的电子转移情况
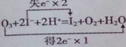 .
.(2)I2可以继续与I-发生反应Ⅱ:I2(aq)+I-(aq)?I3-(aq)△H,为探究外在条件对I3-生成速率的影响,做了如下三组实验,完成表中的内容(表中不要留空格):
| 实验编号 | 实验目的 | 反应物 | 温度 | 反应前溶液的pH |
| A | 对照组 | O3+NaI+H2SO4 | 25℃ | 5.2 |
| B | 研究FeCl2对I3-生成速率的影响 | O3+NaI+H2SO4+FeCl2 | 25℃ | 5.2 |
| C | 研究温度对I3-生成速率的影响 | O3+NaI+H2SO4 | 5℃ | 5.2 |
①反应Ⅱ的△H<0(填“>”“<”或“=”)
②实验B 10s内,I3-的生成速率为8.8×10-4mol/(L.s).
③实验B 18s后,I3-生成速率降低的主要原因是I-浓度降低.
(4)为进一步探究FeCl2对I3-生成速率的影响,提出合理假设,
假设一:Fe2+对反应起催化作用;
假设二:Cl-对反应起催化作用.
(5)请你设计实验验证上述假设一,写出实验步骤及结论.
实验步骤及结论:取一定量NaI溶液,加入稀硫酸调节pH=5.2,将溶液均分为两份A和B,向A、B试管中分解加入等物质的量的FeSO4、Na2SO4固体少许,之后同时向两支试管中通入O3,用离子色谱仪测定10s后I3-浓度,若cA(I3-)>cB(I3-),说明假设一成立,若cA(I3-)=cB(I3-),则假设一不成立.
14.被誉为“矿石熊猫”的香花石,由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法错误的是( )
| A. | 原子半径:Y>Z>R>T | |
| B. | 气态氢化物的稳定性:W<R<T | |
| C. | 最高价氧化物对应的水化物的碱性:X>Z | |
| D. | XR2、WR2两种化合物中R的化合价相同 |
11.下列解释实验现象的反应方程式正确的是( )
| A. | 在CH3COONa溶液中,滴加酚酞变红:CH3COO-+H2O═CH3COOH+OH- | |
| B. | 在H2O2溶液中,滴加FeCl3溶液产生气泡:2H2O2+2Cl-═2H2O+O2↑+Cl2↑ | |
| C. | 将相互接触的铜片和锌片置于稀硫酸中,铜片表面有气泡产生:Cu+2H+═Cu2++H2↑ | |
| D. | 向Cu(OH)2悬浊液中滴加Na2S溶液,蓝色沉淀变黑色:Cu(OH)2(s)+S2- (aq)?CuS(s)+2OH- (aq) |
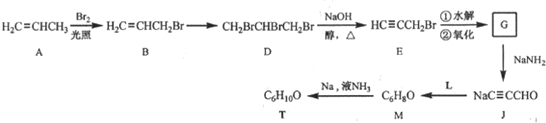
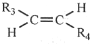 ,则T的结构简式为
,则T的结构简式为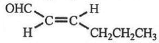 .
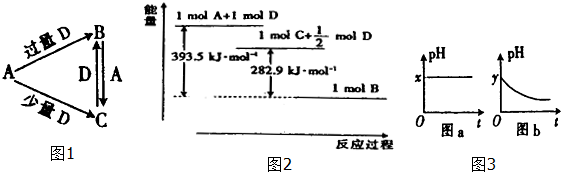
.
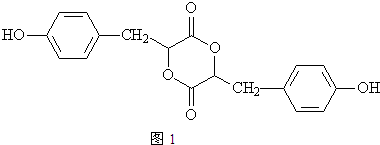

 .
. .
.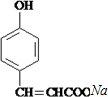 +
+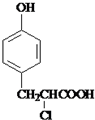 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$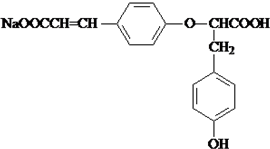 +HCl.
+HCl.