题目内容
10.已知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12.下列关于该温度下的叙述正确的是( )| A. | 向氯化银的悬浊液中加入氯化钠溶液,Ksp(AgCl)减小 | |
| B. | 饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 | |
| C. | 若向0.0008mol•L-1的K2CrO4溶液中加入等体积0.002 mol•L-1的AgNO3溶液,则CrO42--完全沉淀 | |
| D. | 若将0.001mol•L-1AgNO3溶液滴入浓度均为0.001 mol•L-1的KCl和K2CrO4混合溶液中,则先产生AgCl沉淀 |
分析 A、AgCl的Ksp只与温度有关,与离子的浓度有关;
B、饱和AgCl溶液中c2(Ag+)=Ksp(AgCl)=1.56×10-10,饱和Ag2CrO4溶液中$\frac{{c}^{3}(A{g}^{+})}{2}$=Ksp(Ag2CrO4)=1×10-12,由此分析解答;
C、先让两者反应,然后根据剩余银离子,结合溶度积求CrO42-离子的浓度与1.0×10-5mol/L比较;
D、根据Ksp(AgCl)、Ksp(Ag2CrO4),则当Cl-、CrO42-开始沉淀时c(Ag+)各是多少.
解答 解:A、温度不变则Ksp不变,故A错误;
B、饱和AgCl溶液中c2(Ag+)=Ksp(AgCl)=1.56×10-10,饱和Ag2CrO4溶液中$\frac{{c}^{3}(A{g}^{+})}{2}$=Ksp(Ag2CrO4)=1×10-12,显然后者的c(Ag+)大,故B错误;
C、CrO42--完全沉淀则c(CrO42--)≤10-5mol•L-1,此时c(Ag+)≥$\sqrt{\frac{{K}_{sp}(A{g}_{2}Cr{O}_{4})}{c(C{r}_{2}{O}_{4}^{2-})}}$=3.2×10-4mol•L-1,故应向0.0008mol•L-1的K2CrO4溶液中加入等体[3.2×10-4+2(0.0004-10-5)]×2=2.2×10-3mol•L-1,故C错误;
D、饱和AgCl溶液中c(Ag+)比饱和Ag2CrO4溶液中c(Ag+)小,故在同浓度的KCl和K2CrO4混合溶液中滴入AgNO3溶液,先生成AgCl沉淀,故D正确;
故选D.
点评 本题考查溶度积常数的有关计算、判断离子是否完全,沉淀等问题,综合性强,难度较大.

练习册系列答案
相关题目
1.下列各组指定的元素,不能形成AB2型化合物的是( )
| A. | 2s22p3和2s22p4 | B. | 3s23p4和2s22p4 | C. | 3s2和2s22p3 | D. | 3s23p1和3s23p4 |
18.微粒有多种表示方式,下列各组不同表示方式一定代表同种微粒的是( )
| A. | C3H6、CH2═CHCH3 | B. | H2O2、 | C. |  | D. |  1S22S22p63S23p6 1S22S22p63S23p6 |
5.下列有关物质分类正确的是( )
| A. | CuO、MgO、Na2O2均属于碱性氧化物 | B. | 盐酸、醋酸、苯酚均属于强电解质 | ||
| C. | CO2、CCl4、蛋白质均属于有机物 | D. | 液氯、晶体硅、臭氧均属于单质 |
15.如表中的陈述均正确并且前后存在因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水和酸性高锰酸钾溶液褪色 |
| B | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| C | 浓硫酸有吸水性 | 浓硫酸可使蔗糖和纸张碳化变黑 |
| D | SiO2有导电性 | SiO2可用于制备光导纤维 |
| A. | A | B. | B | C. | C | D. | D |
2.对二甲苯(PX)是生产矿泉水瓶(聚对苯二甲酸乙二醇酯,简称PET)的必要原料,生产涉及的反应之一如图所示.下列有关说法错误的是( )
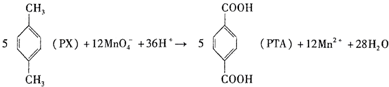

| A. | PX分子中既含σ键又含π键 | |
| B. | PTA是该反应的氧化产物 | |
| C. | PTA与乙二醇通过加聚反应即可生产PET塑料 | |
| D. | 该反应每消耗1molPX,共转移12NA个电子(NA为阿伏伽德罗常数) |
19.构成A、B、C、D、E五种物质的元素中,只有一种不属于短周期元素.A、B、C、D、E五种物质之间的转化关系如图所示:下列判断错误的是( )

| A. | 若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式为(NH4)2SO4 | |
| B. | 若A和B都是盐,A难溶于水,而B易溶于水,D不溶于稀硝酸,C为无色无味气体,则B的化学式为NaHSO4 | |
| C. | 若A是2:1 型的离子化合物,B是硫酸盐,D既可溶于稀盐酸又可溶于NaOH溶液,且A与B的物质的量之比为3:1时恰好完全反应,则B的化学式为Al2(SO4)3 | |
| D. | 若A是1:1型的离子化合物,A与过量的B溶液反应才有D生成;将C燃烧的产物通过装有碱石灰的干燥管或盛有浓硫酸的洗气瓶,两者的质量都增加,则B的化学式一定为Al2(SO4)3 |
20.室温下,将0.2mol•L-1的一元酸HA和0.1mol•L-1的NaOH溶液等体积混合后,溶液显碱性,下列说法不正确的是( )
| A. | 0.1mol•L-1 HA溶液与0.1 mol•L-1的NaOH溶液中,水电离出来的c(H+)相等 | |
| B. | 混合后溶液中:c(HA)>c(Na+)>c(A-)>c(OH-) | |
| C. | 混合后溶液中:c(A-)+c(HA)=0.2 mol•L-1 | |
| D. | 混合后溶液中:c(Na+)+c(H+)=c(A-)+c(OH-) |