题目内容
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
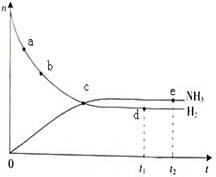
N2(g)+3H2(g)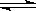 2NH3(g),500℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
2NH3(g),500℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
下列叙述正确的是
N2(g)+3H2(g)
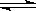 2NH3(g),500℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
2NH3(g),500℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
下列叙述正确的是
| A.点e的正反应速率比点d的大 |
| B.点c处反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不同 |
| D.在给定条件下,t1、t2时刻NH3的含量相同 |
D
根据图像可知,e点和d点都是相同条件下的平衡状态,反应速率是相同的,A、C都不正确。C点正逆反应还是变化的,不属于平衡状态。t1、t2时刻的平衡状态相同,所以氨气的含量相同,因此正确的答案是D。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
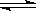 2NH3(g) 达平衡的标志是
2NH3(g) 达平衡的标志是 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )  2HI(g),下列情况一定能说明反应已达到平衡状态的是( )
2HI(g),下列情况一定能说明反应已达到平衡状态的是( ) 4C(g),
4C(g), H >0达到平衡时,改变条件重新达到平衡后体系中A的转化率增大,可行的是 __
H >0达到平衡时,改变条件重新达到平衡后体系中A的转化率增大,可行的是 __
 2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是( )
2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是( ) pC(g),达到平衡时,测得c(C)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(C)为0.3 mol·L-1。则下列判断正确的是( )
pC(g),达到平衡时,测得c(C)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(C)为0.3 mol·L-1。则下列判断正确的是( )