题目内容
.(10分)化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种,且均符合勒夏特列原理。
(1)在固定容积的密闭容器中,反应A(g)+2B(g) 4C(g),
4C(g),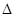 H >0达到平衡时,改变条件重新达到平衡后体系中A的转化率增大,可行的是 __
H >0达到平衡时,改变条件重新达到平衡后体系中A的转化率增大,可行的是 __
A.增加B的物质的量 B.加压 C.升温 D.使用催化剂
(2)某溶液是由体积相等的NaOH溶液和醋酸混合而成,且恰好呈中性,则混合前c(NaOH) ____c(CH3COOH),混合后溶液中c(CH3COO-)____c(Na+)
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒(不考虑Zn粒对反应速率的影响),反应过程中两溶液的pH变化如下图所示。
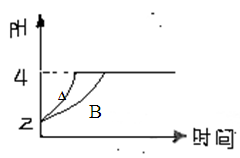
则图中表示醋酸溶液中pH变化曲线的是 (填A或B)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1 m2(选填<﹑=﹑>)
(1)在固定容积的密闭容器中,反应A(g)+2B(g)
 4C(g),
4C(g),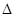 H >0达到平衡时,改变条件重新达到平衡后体系中A的转化率增大,可行的是 __
H >0达到平衡时,改变条件重新达到平衡后体系中A的转化率增大,可行的是 __A.增加B的物质的量 B.加压 C.升温 D.使用催化剂
(2)某溶液是由体积相等的NaOH溶液和醋酸混合而成,且恰好呈中性,则混合前c(NaOH) ____c(CH3COOH),混合后溶液中c(CH3COO-)____c(Na+)
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒(不考虑Zn粒对反应速率的影响),反应过程中两溶液的pH变化如下图所示。

则图中表示醋酸溶液中pH变化曲线的是 (填A或B)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1 m2(选填<﹑=﹑>)
(1)AC(每个1分) (2)< ;= (3)B; <
(1)反应是条件增大、吸热发热可逆反应,所以要增大A的转化率,平衡应该向正反应方向移动,所以选项AC均可以。加压平衡向逆反应方向移动。催化剂不能改变平衡状态。所以正确的答案是AC。
(2)若恰好反应,则生成物醋酸钠水解显碱性,因此要显中性,醋酸一定是过量的。即氢氧化钠的浓度小于醋酸的。
(3)醋酸是弱电解质,存在电离平衡。在反应过程中会继续电离出氢离子,所以醋酸中氢离子的浓度变化程度小于盐酸。因此要使反应后的pH相等,则醋酸需要的时间就多,即B表示醋酸的。醋酸中消耗的氢离子多,则相应的锌消耗的也就多。
(2)若恰好反应,则生成物醋酸钠水解显碱性,因此要显中性,醋酸一定是过量的。即氢氧化钠的浓度小于醋酸的。
(3)醋酸是弱电解质,存在电离平衡。在反应过程中会继续电离出氢离子,所以醋酸中氢离子的浓度变化程度小于盐酸。因此要使反应后的pH相等,则醋酸需要的时间就多,即B表示醋酸的。醋酸中消耗的氢离子多,则相应的锌消耗的也就多。

练习册系列答案
相关题目
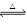 2NH3 (g) ΔH =-92.2 kJ/mol在不同时间段里化学反应速率随时间变化如图所示,据此判断下列说法正确的是
2NH3 (g) ΔH =-92.2 kJ/mol在不同时间段里化学反应速率随时间变化如图所示,据此判断下列说法正确的是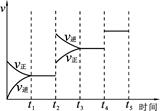
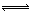 2HI(g); △H<0并达平衡。HI的体积分数
2HI(g); △H<0并达平衡。HI的体积分数 随时间变化如图曲线(II)所示。若改变反应条件,在甲条件下
随时间变化如图曲线(II)所示。若改变反应条件,在甲条件下
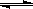 2NH3(g),平衡时测得N2的转化率为12%,则在相同温度和压强下,平衡时混合气体的体积是反应前的
2NH3(g),平衡时测得N2的转化率为12%,则在相同温度和压强下,平衡时混合气体的体积是反应前的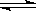 2NH3(g),500℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
2NH3(g),500℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
 N2O4(g)△H<0。
N2O4(g)△H<0。
 2Z(g) 此反应达到平衡的标志是( )
2Z(g) 此反应达到平衡的标志是( ) 2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
2SO3,2 min时,测得O2的物质的量为1.6 mol,则: (1)2min内,平均反应速率v(O2)= ; v(SO3)= 。
(1)2min内,平均反应速率v(O2)= ; v(SO3)= 。 2Z(g )+ W(s) ;△H >0达到平衡,下列判断正确的是( )
2Z(g )+ W(s) ;△H >0达到平衡,下列判断正确的是( )