题目内容
12. 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:T<X | B. | R与Q的电子数相差16 | ||
| C. | 气态氢化物稳定性:R<T<Q | D. | 最高价氧化物的水化物的酸性:T>Q |
分析 R单质在暗处与H2剧烈化合并发生爆炸,则R是F元素,由元素R、X、T、Z、Q在元素周期表中的相对位置,可知X是S元素、T是Cl元素、Z是Ar元素、Q是Br元素.
A.同一周期元素的非金属性随着原子序数的增大而增强,但稀有气体较稳定;
B.R的原子序数是9、Q的原子序数是35;
C.元素的非金属性越强,其氢化物越稳定;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
解答 解:R单质在暗处与H2剧烈化合并发生爆炸,则R是F元素,由元素R、X、T、Z、Q在元素周期表中的相对位置,可知X是S元素、T是Cl元素、Z是Ar元素、Q是Br元素,
A.同一周元素的非金属性随着原子序数的增大而增强,但稀有气体较稳定,所以非金属性T>X,故A错误;
B.R的原子序数是9、Q的原子序数是35,则R与Q的电子数的差=35-9=26,故B错误;
C.元素的非金属性越强,其氢化物越稳定,非金属性R>T>Q,所以氢化物的稳定性R>T>Q,故C错误;
D.同主族自上而下非金属性减弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强,故最高价氧化物的水化物的酸性:T>Q,故D正确,
故选D.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,正确推断元素是解本题关键,注意理解掌握同主族元素原子序数关系,注意F元素没有最高价含氧酸.

练习册系列答案
相关题目
2.下列叙述中错误的是( )
| A. | 点燃前甲烷不必验纯 | |
| B. | 甲烷燃烧能放出大量的热,所以是一种很好的气体燃料 | |
| C. | 煤矿的矿井要注意通风和严禁烟火,以防爆炸事故的发生 | |
| D. | 甲烷是一种具有正四面体结构的很稳定的气体 |
3.部分弱酸的电离平衡常数如表:
下列选项正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡 常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 2CN-+H2O+CO2═2HCN+CO32- | |
| B. | 2HCOOH+CO32-═2HCOO-+H2O+CO2↑ | |
| C. | 等浓度的HCOONa和NaCN溶液的pH前者大于后者 | |
| D. | 中和等浓度的HCOOH和HCN消耗NaOH的量前者等于后者 |
20.下列图中所示的操作一般不用于进行物质的分离或提纯的是( )
| A. |  | B. | 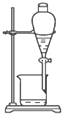 | ||
| C. | 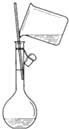 | D. | 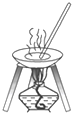 |
17.11.2L甲烷、乙烷、甲醛组成的混合气体,完全燃烧后生成15.68LCO2(气体体积均在标准状况下测定),混合气体中乙烷的体积百分含量为( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
4.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| C. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| D. | 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
1.某无色气体X,可能含有CO2、SO2、HCl、HBr中的一种或几钟.将X通过适量的氯水时,X完全被吸收.将所得的无色溶液分装于两支试管后,分别加入酸化AgNO3与BaCl2溶液,结果均产生白色沉淀.下列推论正确的是( )
| A. | X中可能有HBr | B. | X中一定有SO2 | C. | X中可能有CO2 | D. | X中一定有HCl |
2.由下列结构片段组成的蛋白质在胃液中水解,不可能产生的氨基酸是( )
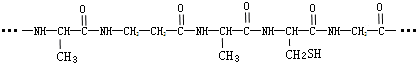

| A. | 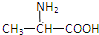 | B. | H2NCH2COOH | C. | 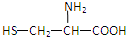 | D. | 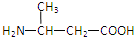 |