题目内容
在高中我们将从元素原子得失电子的角度来认识氧化还原反应,而元素原子得失电子表现为元素化合价的变化.因此可以把元素化合价有升降的化学反应确定为氧化还原反应,据此可判断下列化学反应不属于氧化还原反应的是( )
| A、Zn+CuSO4=ZnSO4+Cu | ||||
B、CuO+CO
| ||||
| C、Na2CO3+2HCl=2NaCl+H2O+CO2↑ | ||||
D、2KClO3
|
考点:氧化还原反应
专题:氧化还原反应专题
分析:存在元素化合价变化的反应,为氧化还原反应;反之,不存在元素的化合价变化,则不属于氧化还原反应,以此来解答.
解答:
解:A.Zn、Cu元素的化合价变化,属于氧化还原反应,故A不选;
B.Cu、C元素的化合价变化,属于氧化还原反应,故B不选;
C.没有元素的化合价变化,不属于氧化还原反应,故C选;
D.Cl、O元素的化合价变化,属于氧化还原反应,故D不选;
故选C.
B.Cu、C元素的化合价变化,属于氧化还原反应,故B不选;
C.没有元素的化合价变化,不属于氧化还原反应,故C选;
D.Cl、O元素的化合价变化,属于氧化还原反应,故D不选;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
对以下化学问题的解释中错误的是( )
| A、工业盐酸显黄色,是由于含有杂质FeCl3 |
| B、碘化钾溶液久置显黄色,是由于I被氧化,析出的I2溶于溶液中 |
| C、浓硝酸显黄色,是由于硝酸见光分解生成的NO2溶液酸液中 |
| D、炼钢是在高温下利用还原剂除去生铁中的杂质 |
对实验A-D的实验现象预测正确的是( )
A、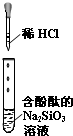 试管中红色溶液逐渐变成无色溶液 |
B、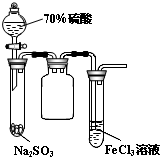 试管中出现淡黄色浑浊 |
C、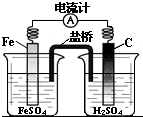 铁棒上有无色气泡产生 |
D、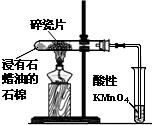 酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
对于反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4来说,下列结论正确的是( )
| A、FeS2既是氧化剂,又是还原剂 |
| B、只有CuSO4作氧化剂 |
| C、被氧化的硫和被还原的硫质量比是3:7 |
| D、被氧化的硫和被还原的硫质量比是1:1 |
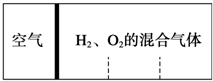 如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的
如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的| 1 |
| 4 |
| A、2:7 | B、5:4 |
| C、2:1 | D、4:5 |
下列叙述正确的是( )
| A、元素处于最高价态时一定有强氧化性;同理元素处于最低价态时一定具有强还原性 |
| B、将FeCl2溶液与稀HNO3混合离子反应方程式:Fe2++4H++NO3-═Fe3++NO↑+2H2O |
| C、HF、Al(OH)3、氨水都是弱电解质 |
| D、颜色反应、显色反应、指示剂变色反应均属化学变化 |
下列叙述中全部为不正确的组合是( )
(1)纯铁比碳素钢易生锈
(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C(碳)>Si
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
(11)用浸泡过的高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
(12)同周期金属元素的化合价越高,其原子失电子能力越弱.
(1)纯铁比碳素钢易生锈
(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C(碳)>Si
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
(11)用浸泡过的高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
(12)同周期金属元素的化合价越高,其原子失电子能力越弱.
| A、(1)(4)(5)(6)(7)(11) |
| B、(2)(3)(5)(7)(9)(12) |
| C、(1)(2)(3)(4)(7)(10) |
| D、(2)(6)(8)(10)(11)(12) |