题目内容
【题目】乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室用CH3COOH (60g/mol)和CH3CH2CH2CH2OH(74g/mol)在浓硫酸加热条件下制备乙酸正丁酯(116g/mol)。
主要实验步骤如下:


Ⅰ合成:
在干燥的圆底烧瓶中加11.5mL(9.25g,0.125mol)正丁醇、7.2mL(12.0g,0.2mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1示装置安装好.在分水器中预先加入5.00mL水,其水面低于分水器回流支管下沿3~5mm,然后用小火加热,反应大约40min.
Ⅱ分离与提纯:
①将烧瓶中反应后的混后物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10mL水,10mL10%碳酸钠溶液洗至无酸性(pH=7),充分振荡后静置,分去水层
②将酯层倒入小锥形瓶中,加少量无水硫酸镁
③过滤,将乙酸正丁酯粗产品转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数如下:

根据以上信息回答下列问题:
(1)制备乙酸正丁酯的化学方程式为:__________________________________ ,制备过程中易生成副产物正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3),该副反应的化学方程式为:___________。
(2)图1整个装置可看作由分水器、圆底烧瓶和______(填仪器名称)组成,其中冷水应从______(填a或b)管口通入.分水器可将生成的水从反应体系中分离出来,有利于______,如何判断该合成反应达到了终点:_____________________。
(3)在操作步骤①时,用右手压住分液漏斗的玻璃塞,左手握住旋塞将分液漏斗倒转过来,用力振荡,振摇几次后要放气,放气时支管口不能对着人和火.在操作步骤②加入无水硫酸镁的作用是________ 。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(双选)。
A.水B.甘油(沸点290℃) C.砂子D.石蜡油(沸点200~300℃)
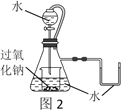
如果蒸馏装置如图2所示,则收集到的产品中可能混有______杂质。
(5)反应结束后,生成11.6g乙酸正丁酯,则正丁醇的转化率约为______。
【答案】CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O 2CH3CH2CH2CH2OH
CH3COOCH2CH2CH2CH3+H2O 2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O (球形)冷凝管 b 反应向正向进行,提高反应物转化率 分水器中水面不再升高 干燥 BD 正丁醚 80%
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O (球形)冷凝管 b 反应向正向进行,提高反应物转化率 分水器中水面不再升高 干燥 BD 正丁醚 80%
【解析】
(1)乙酸和正丁醇在浓硫酸作用下发生酯化反应生成乙酸正丁酯和水;正丁醇之间发生反应生成正丁醚和水;
(2)由装置图可知,装置由分水器、圆底烧瓶和冷凝管组成;冷凝时,应尽量使冷凝水充满冷凝管,以充分冷凝;酯化反应为可逆反应,分离出生成物有利于平衡正向移动,当反应物、生成物的浓度、物质的量等不再改变时达到平衡状态;
(3)产品有水考虑干燥;
(4)乙酸正丁酯的沸点为126.1℃,选择沸点稍高的液体加热;正丁醇和乙酸易溶于水,在用水洗、10%碳酸钠溶液洗时,已经被除去,则乙酸正丁酯的杂质为正丁醚;
(5)产率=![]() 计算得到。
计算得到。
(1)乙酸与正丁醇反应生成乙酸正丁酯和水,其反应方程式:CH3COOH+HO(CH2)3CH3 ![]() CH3COO(CH2)3CH3+H2O,正丁醇之间发生反应生成正丁醚和水,反应方程式为:2CH3CH2CH2CH2OH
CH3COO(CH2)3CH3+H2O,正丁醇之间发生反应生成正丁醚和水,反应方程式为:2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O;
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O;
故答案为:CH3COOH+HO(CH2)3CH3 ![]() CH3COO(CH2)3CH3+H2O;2CH3CH2CH2CH2OH
CH3COO(CH2)3CH3+H2O;2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O;
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O;
(2)由装置图可知,装置由分水器、圆底烧瓶和冷凝管组成;冷凝管中的冷凝水应该从下口进上口出,所以从b管口通入;酯化反应为可逆反应,分离出生成物有利于平衡正向移动,当反应物、生成物的浓度、物质的量等不再改变时达到平衡状态,则分水器中的水层不再增加时,视为反应的终点;
故答案为:冷凝管;b;反应向正向进行,提高反应物转化率;分水器中水面不再升高;
(3)反应生成的酯有水分,所以要用无水硫酸镁干燥;
故答案为:干燥;
(4)乙酸正丁酯的沸点为126.1℃,选择沸点稍高的液体加热,所以可以在甘油和石蜡油中加热,水的沸点为100℃,加热温度太低,用砂子加热温度太高不易控制;正丁醇和乙酸易溶于水,在用水洗、10%碳酸钠溶液洗时,已经被除去,正丁醚与乙酸丁酯互溶,水洗和10%碳酸钠溶液洗时不能除去,所以蒸馏时会有少量挥发进入乙酸丁酯,则乙酸正丁酯的杂质为正丁醚;
故答案为:BD;正丁醚;
(5)CH3COOH+HO(CH2)3CH3 ![]() CH3COO(CH2)3CH3+H2O,则理论上应生成酯为0.125mol,实际生成11.6g,所以乙酸正丁酯的产率为
CH3COO(CH2)3CH3+H2O,则理论上应生成酯为0.125mol,实际生成11.6g,所以乙酸正丁酯的产率为![]() =80%,
=80%,
故答案为:80%。