题目内容
16.向某无色溶液中加入铝片能放出氢气,则此溶液中一定能大量共存的离子组是( )| A. | Ba2+、Cl-、Na+、K+ | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、SO32-、Cl-、NO3- | D. | Fe3+、Na+、AlO2-、SO42- |
分析 无色溶液中不存在有色的离子;加入铝片放出氢气的溶液为酸性或强碱性溶液,溶液中存在大量氢离子或氢氧根离子,
A.四种离子之间不反应,都是无色离子,都不与氢离子和氢氧根离子反应;
B.碳酸氢根离子能够与氢离子和氢氧根离子反应;
C.酸性条件下,硝酸根离子能够氧化亚硫酸根离子;
D.铁离子为有色离子,不满足溶液无色的条件;且铁离子与氢氧根离子、偏铝酸根离子反应,偏铝酸根离子与氢离子反应.
解答 解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;加入铝片放出氢气的溶液为酸性或强碱性溶液,
A.Ba2+、Cl-、Na+、K+之间不发生反应,都为无色离子,且都不与氢离子和氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.HCO3-能够与氢离子和氢氧根离子反应,在溶液中一定不能大量共存,故B错误;
C.SO32-、NO3-在酸性条件下能够发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.Fe3+为有色离子,Fe3+、AlO2-之间发生双水解反应,在溶液中一定不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
6.在Zn、ZnO、ZnCO3、盐酸、CuCl2和CaCl2溶液六种物质中,每两种物质反应能生成ZnCl2的方法有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
4.下列操作能促进水的电离,且使溶液的pH>7的是( )
| A. | 将纯水加热到90℃ | B. | 向水中加少量Na2CO3溶液 | ||
| C. | 向水中加少量NaOH溶液 | D. | 向水中加少量FeCl3溶液 |
1.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 化合物AE与CE有相同类型的化学键 |
5.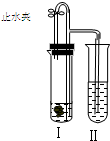 如图所示装置进行实验(图中铁架台等仪器均已略去).在Ⅰ中加入试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出;一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊.不符合以上实验现象的Ⅰ和Ⅱ中应加入的试剂是( )
如图所示装置进行实验(图中铁架台等仪器均已略去).在Ⅰ中加入试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出;一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊.不符合以上实验现象的Ⅰ和Ⅱ中应加入的试剂是( )
 如图所示装置进行实验(图中铁架台等仪器均已略去).在Ⅰ中加入试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出;一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊.不符合以上实验现象的Ⅰ和Ⅱ中应加入的试剂是( )
如图所示装置进行实验(图中铁架台等仪器均已略去).在Ⅰ中加入试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出;一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊.不符合以上实验现象的Ⅰ和Ⅱ中应加入的试剂是( )| A | B | C | D | |
| Ⅰ | CaCO3、稀HCl | Fe、稀H2SO4 | NaHCO3、稀H2SO4 | Al、稀NaOH |
| Ⅱ | AgNO3 | NaOH | MgCl2 | AlCl3 |
| A. | A | B. | B | C. | C | D. | D |
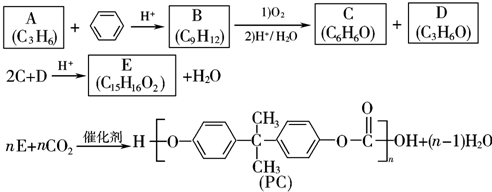
 .
. .
. (写出结构简式).
(写出结构简式).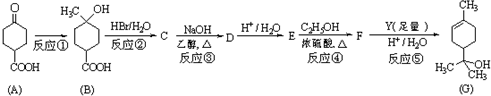
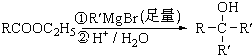
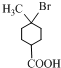 +2NaOH
+2NaOH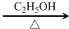
 +NaBr+2H2O.
+NaBr+2H2O.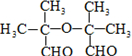 .
.