��Ŀ����
��ʢ��KI��Һ���Թ��м�������CCl4��μ���ˮ��CCl4������ɫ������������Թ��еμ���ˮ����CCl4�����dz���������ɫ�����������գ�
��1��д������ƽCCl4������ɫ�����ɫ�Ļ�ѧ��Ӧ����ʽ�����ϵ����l��������д���� ___��+___��+___�ڡ�__HIO3+__��
��2�����������еĻ�ԭ����______��
��3����KI����KBr����CCl4���Ϊ____ɫ�������μ���ˮ��CCl4�����ɫû�б仯��Cl2��HIO3��HBrO3��������ǿ������˳����_________��
��4���ӵ����к�����Ϊ20 mg-50 mg��kg����ȡ�ӵ��Σ���KIO3��ʳ�Σ�1000 kg������Kl��Cl2��Ӧ��KIO3��������Ҫ����Cl2_____L����״��������2λС������
��1��д������ƽCCl4������ɫ�����ɫ�Ļ�ѧ��Ӧ����ʽ�����ϵ����l��������д���� ___��+___��+___�ڡ�__HIO3+__��
��2�����������еĻ�ԭ����______��
��3����KI����KBr����CCl4���Ϊ____ɫ�������μ���ˮ��CCl4�����ɫû�б仯��Cl2��HIO3��HBrO3��������ǿ������˳����_________��
��4���ӵ����к�����Ϊ20 mg-50 mg��kg����ȡ�ӵ��Σ���KIO3��ʳ�Σ�1000 kg������Kl��Cl2��Ӧ��KIO3��������Ҫ����Cl2_____L����״��������2λС������
��1��I2+5Cl2+6H2O��2HIO3+10HCl
��2��KI��I2
��3�����أ�HBrO3>Cl2>HIO3
��4��10.58
��2��KI��I2
��3�����أ�HBrO3>Cl2>HIO3
��4��10.58

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
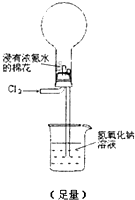 ͨ������������Һ���û���Ӧ���ԱȽϽ�����ԭ�Ե�ǿ����ͨ���ǽ�������û���Ӧ��Ҳ���ԱȽϷǽ��������Ե�ǿ����
ͨ������������Һ���û���Ӧ���ԱȽϽ�����ԭ�Ե�ǿ����ͨ���ǽ�������û���Ӧ��Ҳ���ԱȽϷǽ��������Ե�ǿ����

