题目内容
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色.
完成下列填空:
1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

写出产物即可不需要配平
2)整个过程中的还原剂是
3)把KI换成KBr,则CCl4层变为
完成下列填空:
1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

写出产物即可不需要配平
2)整个过程中的还原剂是
I2
I2
.3)把KI换成KBr,则CCl4层变为
棕
棕
色:继续滴加氯水,CCl4层的颜色没有变化. 由此推测Cl2、HIO3、HBrO3氧化性由强到弱的顺序是HBrO3>Cl2>HIO3
HBrO3>Cl2>HIO3
.分析:(1)根据反应现象和I2的性质分析;
(2)根据化合价变化判断氧化剂和还原剂;
(3)氧化剂和还原剂反应生成氧化产物和还原产物,氧化剂氧化性大于氧化产物的氧化性,以此分析.
(2)根据化合价变化判断氧化剂和还原剂;
(3)氧化剂和还原剂反应生成氧化产物和还原产物,氧化剂氧化性大于氧化产物的氧化性,以此分析.
解答:解:(1)氯气具有强氧化性,向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色,说明生成I2,继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色,说明I2被进一步氧化,生成HIO3,同时氯气被还原为HCl,反应的方程式为5Cl2+I2+6H20=2HIO3+10HCl,
故答案为:5Cl2+I2+6H20=2HIO3+10HCl;
(2)在Cl2+I2+H20→HIO3+HCl反应,I元素的化合价升高,被氧化,I2在反应中做还原剂,
故答案为:I2;
(3)氯气的氧化性比溴强,将KI换成KBr,则生成Br2,则CCl4层变为棕色,继续滴加氯水,CCl4层的颜色没有变化,说明氧化性HBrO3>Cl2,根据氧化剂和还原剂反应生成氧化产物和还原产物,氧化剂氧化性大于氧化产物的氧化性,
则有Cl2>HIO3,所以氧化性顺序为HBrO3>Cl2>HIO3,故答案为:棕;HBrO3>Cl2>HIO3;
故答案为:5Cl2+I2+6H20=2HIO3+10HCl;
(2)在Cl2+I2+H20→HIO3+HCl反应,I元素的化合价升高,被氧化,I2在反应中做还原剂,
故答案为:I2;
(3)氯气的氧化性比溴强,将KI换成KBr,则生成Br2,则CCl4层变为棕色,继续滴加氯水,CCl4层的颜色没有变化,说明氧化性HBrO3>Cl2,根据氧化剂和还原剂反应生成氧化产物和还原产物,氧化剂氧化性大于氧化产物的氧化性,
则有Cl2>HIO3,所以氧化性顺序为HBrO3>Cl2>HIO3,故答案为:棕;HBrO3>Cl2>HIO3;
点评:本题考查氯气的性质以及氧化性的强弱比较,题目难度不大,本题易错点为(1).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
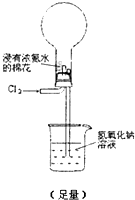 通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.
通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.
