题目内容
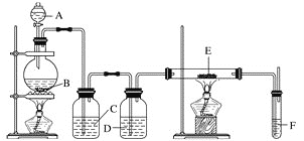
【题目】下列图示与对应的叙述相符合的是
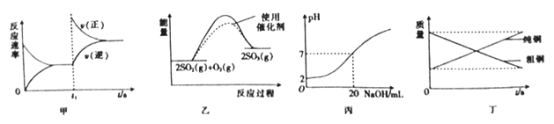
A.图甲表示t1时刻增加反应物浓度后v(正)和v(逆)随时间的变化
B.图乙表示反应2SO2(g)+O2(g)=2SO3(g) △H<0 在两种条件下物质能量随反应过程的变化
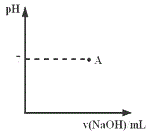
C.图丙表示25℃时用0.01mol/LNaOH溶液滴定20.00 mL 0.01mol/LHCl溶液时pH随NaOH 溶液体积的变化
D.图丁表示电解精炼铜时纯铜和粗铜的质量随时间的变化
【答案】A
【解析】
A.增加反应物浓度后,正反应速率突然增大,但刚开始,生成物浓度不变,逆反应速率不变,然后逐渐反应达到平衡,故A正确;
B. 2SO2(g)+O2(g)=2SO3(g) △H<0反应为放热反应,与图像不符,图中反应为吸热反应,故B错误;
C. 25℃时用0.01mol/LNaOH溶液滴定20.00mL0.01mol/LHCl溶液时,在氢氧化钠溶液体积为20mL时会发生pH的突变,图像未体现,故C错误;
D.电解精炼铜时,阳极溶解的金属除了铜,还有铁、锌等,阴极只析出铜,因此纯铜和粗铜的质量变化与图像不符,粗铜溶解的质量与纯铜增大的质量不等,故D错误;
故选A。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】下列有关离子晶体的数据大小比较不正确的是
A. 熔点:NaF>MgF2>AlF3B. 晶格能:NaF>NaCl>NaBr
C. 阴离子的配位数:CsCl>NaClD. 硬度:MgO>CaO>BaO
【题目】某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为![]() 。
。
阳离子 |
|
阴离子 |
|
甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在无色火焰上灼烧,未出现黄色火焰
②取少量溶液,加入![]() 溶液无明显变化。
溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
④向③中所得的溶液中加入![]() 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
(1)步骤①使用的焰色反应属于___(填“物理”或“化学”)变化
(2)③中加入少量盐酸生成无色气体的离子方程式是____
(3)该溶液中一定含有的阳离子有___,一定含有的阴离子有___
(4)检验溶液中存在![]() 的方法是_____
的方法是_____
(5)取![]() 该溶液,向溶液中加入过量的稀氢氧化钠溶液,充分反应后,过滤、洗涤,将沉淀在空气中灼烧后得到的固体质量为___g
该溶液,向溶液中加入过量的稀氢氧化钠溶液,充分反应后,过滤、洗涤,将沉淀在空气中灼烧后得到的固体质量为___g