题目内容
【题目】下列有关离子晶体的数据大小比较不正确的是
A. 熔点:NaF>MgF2>AlF3B. 晶格能:NaF>NaCl>NaBr
C. 阴离子的配位数:CsCl>NaClD. 硬度:MgO>CaO>BaO
【答案】A
【解析】
A.离子半径Na+>Mg2+>Al3+,离子半径越小,电荷越多,晶格能越大,则熔点越高,故A错误;
B.离子半径Br->Cl->F-,离子半径越小,所带电荷数越大,晶格能越大,故B正确;
C.NaCl、CsCl的晶胞结构分别为: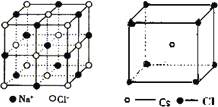 ,结合图可知,CsCl为立方体心结构,Cl-的配位数是8;NaCl为立方面心结构,钠离子的配位数为6,Cl-的配位数是6,则阴离子的配位数:CsCl>NaCl,故C正确;
,结合图可知,CsCl为立方体心结构,Cl-的配位数是8;NaCl为立方面心结构,钠离子的配位数为6,Cl-的配位数是6,则阴离子的配位数:CsCl>NaCl,故C正确;
D.原子半径Ba>Ca>Mg,原子半径越大,键能越小,硬度越小,故D正确。
答案选A。

【题目】(1)已知在常温常压下:
①CH3OH(l)+ O2(g)=CO(g)+ 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:___________________________ 。
(2)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
容器 | 甲 |
反应物投入量 | 1mol CO2(g)和3mol H2(g) |
平衡时c(CH3OH) | c1 |
平衡时能量变化 | 放出29.4kJ |
若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是_____mol/(L·s)。
(3)铅蓄电池放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。铅蓄电池放电时的正极反应式为____ ,当电路中有0.2mol电子转移时,理论上两电极质量变化的差为_______ g。
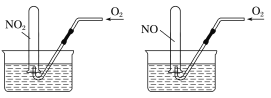
(4)甲烷可直接应用于燃料电池,该电池采用可传导O2-的固体氧化物为电解质,其工作原理如图所示:
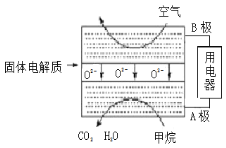
①A极电极反应式为____________________。
②若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中O2体积为20%),则理论上消耗甲烷________mol。