题目内容
14.下列两种气体的分子数一定相等的是( )| A. | 等温等体积的O2和N2 | B. | 等压等体积的N2和CO2 | ||
| C. | 质量相等、密度不等的N2和C2H4 | D. | 体积相等、密度不等的CO和C2H4 |
分析 两种气体的分子数一定相等,根据N=nNA可知,二者物质的量相等,
A.根据PV=nRT,可知温等体积下压强影响气体物质的量;
B.根据PV=nRT,可知等压等体积下温度影响气体物质的量;
C.N2和C2H4的摩尔质量都是28g/mol,根据物质的量n=$\frac{m}{M}$进行判断;
D.根据m=ρV、n=$\frac{m}{M}$进行计算.
解答 解:两种气体的分子数一定相等,根据N=nNA可知,二者物质的量相等,
A.根据PV=nRT可知,等温等体积下影响气体物质的量的因素为压强,二者压强不一定相等,故含有分子数目不一定相等,故A错误;
B.根据PV=nRT可知,等压等体积下影响气体物质的量的因素为温度,二者温度不一定相等,故含有分子数目不一定相等,故B错误;
C.N2和C2H4的摩尔质量都是28g/mol,二者质量相等,根据n=$\frac{m}{M}$可知二者物质的量相等,故C正确;
D.等体积、不同密度的CO和C2H4,根据m=ρV可知二者质量不相等,但二者摩尔质量相等,再根据n=$\frac{m}{M}$可知物质的量不等,含有分子数目不相等,故D错误;
故选C.
点评 本题考查阿伏伽德罗定律及推论,为高频考点,题目难度中等,把握pV=nRT理解阿伏伽德罗定律及推论为解答的关键,侧重分析与应用能力的考查,注意气体体积与温度、压强有关.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
4.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | W、Z、Y、X的原子半径依次减小 | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的弱 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |
2.甲、乙、丙均为中学化学常见气体单质,A、B、C为常见的化合物.可供参考的信息有:

(I)A和B都极易溶于水,用两根玻璃棒分别蘸A和B的浓溶液后相互靠近,会看到白烟.
(II)甲与乙在一定条件下反应的有关数据为:
分析上述信息回答下列问题:
(1)丙的电子式为:
(2)甲与乙反应生成A的速率为:v(甲)=0.6mol/(L•s).
(3)写出C与NaOH溶液反应生成A的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$H2O+NH3↑.

(I)A和B都极易溶于水,用两根玻璃棒分别蘸A和B的浓溶液后相互靠近,会看到白烟.
(II)甲与乙在一定条件下反应的有关数据为:
| 项目 | 甲 | 乙 | A |
| 起始时 | 3mol/L | 3mol/L | 0 |
| 2s末 | 1.8mol/L | 2.6mol/L | 0.8mol/L |
(1)丙的电子式为:

(2)甲与乙反应生成A的速率为:v(甲)=0.6mol/(L•s).
(3)写出C与NaOH溶液反应生成A的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$H2O+NH3↑.
9.百服宁口服液为解热镇痛药,主要用于治疗头痛、发烧.其主要化学成分的结构简式为:
下列有关该有机物叙述正确的是( )

下列有关该有机物叙述正确的是( )
| A. | 分子式为C8H10NO2 | |
| B. | 该有机物是苯酚的同系物 | |
| C. | 其属于α-氨基酸的同分异构体有3种 | |
| D. | 该有机物可与FeCl3溶液发生显色反应 |
6.分子式为C5H10Cl2的有机分子中,所含有的甲基数不可能为( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
12.短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示.下列说法不正确的是( )


| A. | 原子半径:Y>Z>X | |
| B. | 若Y的氧化物为两性氧化物,则Z的一种单质在空气中易自燃 | |
| C. | 若X的气态氢化物与Z的最高价氧化物的水化物能反应,则生成的盐仅有一种 | |
| D. | 若Y与Z的核电荷数之和为X的4倍,则X、Y、Z的氢化物分子的立体构型分别为:V形,三角锥形,直线形 |
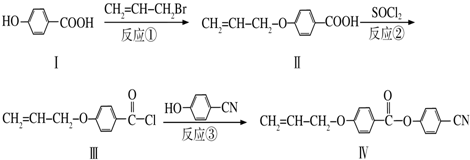
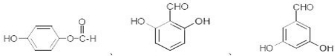 任一种.
任一种.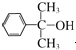 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是 .
.