题目内容
【题目】纳米CaCO3作为工业上重要的无机填充材料,广泛应用于橡胶、塑料、涂料、油墨和造纸等行业。某化学兴趣小组在实验室中利用下列装置模拟工业制备纳米CaCO3.
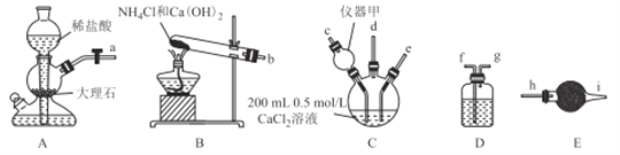
请回答下列问题:
(1)仪器甲的名称是________,在该实验中,其作用是_____.
(2)将上述接口连接顺序补充完整:a![]() ;b
;b![]() ;d
;d![]() 。__________
。__________
(3)装置D中选择的试剂是__________(填序号,下同),装置E中选择的试剂是__________
①饱和Na2CO3溶液 ②饱和NaHCO3溶液 ③无水CaCl2固体 ④碱石灰
(4)装置C中发生反应的离子方程式为__________
(5)随着气体的通入,三颈烧瓶中产生白色沉淀且逐渐增多,但一段时间后,白色沉淀逐渐减少,其可能的原因为_______(结合化学用语解释)。
(6)当生成5g沉淀时,理论上消耗两种气体(标准状况下)的总体积可能为_________
(7)已知:常温下,Ksp(CaCO3)=2.8×10-9,Ksp(CaSO3)=1.4×10-7。向浓度为1.0mol/L的Na2SO3溶液中加入纳米CaCO3,若使CaCO3向CaSO3转化,则该混合液中c(SO32-)/c(CO32-)的值(x)的取值范围为__________。
【答案】 干燥管 防止倒吸 fge、c、h ② ③ Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+ CaCO3+CO2+H2O=Ca(HCO3)2,Ca(HCO3)2易溶于水 3.36L、7.84L x>50
【解析】根据装置图及使用的试剂可知,A是生成二氧化碳的装置;B是生成氨气的装置;C是生成碳酸钙沉淀的装置;生成的二氧化碳中混有氯化氢,可以通过D装置除去,E装置可以防止未反应的氨气污染空气。
(1)根据图示,仪器甲为干燥管,在该实验中,干燥管可以防止三颈烧瓶中气体的压强变化引起的倒吸,故答案为:干燥管;防止倒吸;
(2)根据上述分析,生成的二氧化碳和氨气通入C中反应生成碳酸钙,通过D除去二氧化碳中的氯化氢,尾气用E吸收,上述接口连接顺序为:a→f→g→e;b→c;d →h,故答案为:f→g→e;c;h;
(3)装置D是除去二氧化碳中的氯化氢,可以选择饱和NaHCO3溶液,装置E是吸收未反应的氨气,可以选用无水CaCl2固体,故答案为:②;③;
(4)装置C中氯化钙和氨气、二氧化碳反应生成氯化铵和碳酸钙,反应的离子方程式为Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+,故答案为:Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+;
(5)碳酸钙能够被过量的二氧化碳转化为碳酸氢钙,CaCO3+CO2+H2O=Ca(HCO3)2,Ca(HCO3)2易溶于水,因此随着气体的通入,三颈烧瓶中产生白色沉淀且逐渐增多,但一段时间后,白色沉淀逐渐减少,故答案为:CaCO3+CO2+H2O=Ca(HCO3)2,Ca(HCO3)2易溶于水;
(6)n(CaCl2)=0.2L×0.5 mol/L=0.1mol,5g碳酸钙沉淀的物质的量=![]() =0.05mol,根据Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+可知,当氯化钙过量,消耗氨气0.1mol,二氧化碳0.05mol,共消耗气体0.15mol,标准状况下的体积=0.15mol×22.4L/mol=3.36L;但通入的气体过量将生成的部分碳酸钙溶解,则生成0.1mol碳酸钙消耗氨气0.2mol,二氧化碳0.1mol,溶解0.05mol碳酸钙需要消耗0.05mol二氧化碳,共消耗气体0.35mol,标准状况下的体积=0.35mol×22.4L/mol=7.84L,故答案为:3.36L、7.84L;
=0.05mol,根据Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+可知,当氯化钙过量,消耗氨气0.1mol,二氧化碳0.05mol,共消耗气体0.15mol,标准状况下的体积=0.15mol×22.4L/mol=3.36L;但通入的气体过量将生成的部分碳酸钙溶解,则生成0.1mol碳酸钙消耗氨气0.2mol,二氧化碳0.1mol,溶解0.05mol碳酸钙需要消耗0.05mol二氧化碳,共消耗气体0.35mol,标准状况下的体积=0.35mol×22.4L/mol=7.84L,故答案为:3.36L、7.84L;
(7)向浓度为1.0mol/L的Na2SO3溶液中加入纳米CaCO3,若使CaCO3向CaSO3转化需要满足c(SO32-) c(Ca2+)>Ksp(CaSO3),即c(SO32-)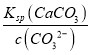 >Ksp(CaSO3),则
>Ksp(CaSO3),则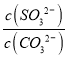 >
>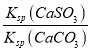 =
=![]() =50,故答案为:x>50。
=50,故答案为:x>50。