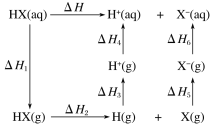
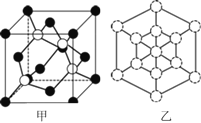
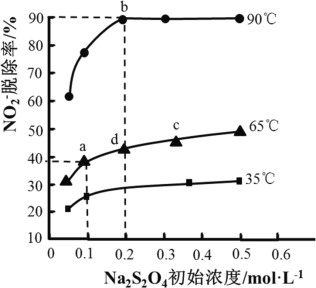
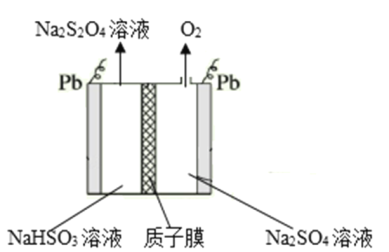
题目内容
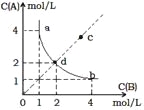
【题目】ToC时,在一固定容积的密闭容器中发生反应:A(g)+B(g)![]() X(s) H < 0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,则判断正确的是
X(s) H < 0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,则判断正确的是
A.ToC时,该反应的平衡常数值为4
B.c点没有达到平衡,此时反应向逆向进行
C.若c点为平衡点,则此时容器内的温度高于ToC
D.ToC时,在d点加入一定量X可达到c点
【答案】C
【解析】
A、该曲线表示平衡时A、B的浓度,取d点,c(A)=c(B)=2mol/L,则K=![]() =
=![]() =
=![]() ,选项A错误;
,选项A错误;
B、c点不是平衡点,A或B的浓度偏高,Qc<K,反应向正方向进行,选项B错误;
C、若c点为平衡点,应该是原平衡向逆方向进行,升温可以达到目的,选项C正确;
D、X为固体,增大X的量不改变平衡的移动,选项D错误;
故选C。

练习册系列答案
相关题目
【题目】不同温度下,反应![]() 的平衡常数如下:
的平衡常数如下:
温度 | 207 | 387 |
平衡常数 |
|
|
下列说法正确的是( )
A.其正反应的![]()
B.207℃时,密闭容器中进行的该反应总压不变不可以作为该反应达到平衡的标志
C.387℃时,1L密闭容器中投入![]() mol的
mol的![]() ,平衡时转化率为
,平衡时转化率为![]()
D.387℃时,1L密闭容器中充入![]()
![]() mol、
mol、![]()
![]() mol和
mol和![]()
![]() mol,则反应将向正反应方向进行
mol,则反应将向正反应方向进行