题目内容
【题目】一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:A(g)+2B(g)![]() 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2υ正(A)=υ逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2)K和x的关系满足K=______________。在保证A浓度不变的情况下,扩大容器的体积,平衡________(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
(3)该反应的逆反应速率与时间的关系如图所示。
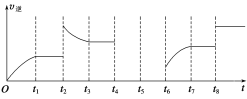
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时__________________;t8时_________________________。
②t2时平衡向________(填“正反应”或“逆反应”)方向移动。
【答案】BC Vx2/n(1-x)3 C 升温或增大C的浓度 使用催化剂 逆反应
【解析】
(1)平衡状态的判断依据是正逆反应速率相等,各组分的浓度保持不变;用三段式分析计算;根据外界条件对化学平衡的影响分析。
(2)根据三段式计算平衡浓度,结合平衡常数概念计算得到平衡常数;根据浓度商与K的关系判断。
(3)①由于纵坐标只表示υ逆,为了便于求解,在解题时可把υ正补上,t2时平衡逆向移动,采用的条件可以是升温或增大C的浓度;t8时平衡不移动,采用的条件是使用了催化剂。
②t2时逆反应速率突然增大,后逐渐减小达到新平衡,且新平衡时反应速率大于原平衡时反应速率,平衡向逆反应方向移动。
(1)A.反应物A与B加入的物质的量之比等于其化学计量数之比,所以平衡后A与B的转化率之比1: 1,故A错误;
B.A的转化率为x,则平衡后有A、B、C物质的量分别为(n-nx)mol、(2n-2nx)mol、 2nxmol, 平衡后气体总物质的量为(3n-nx)mol,恒容容器中,气体物质的量之比等于其压强之比,故B正确;
C.当2υ正(A)=υ逆(B)时,说明正逆反应速率相等,反应达到平衡状态,故C正确;
D. 恒容容器中,充入惰性气体(如Ar) ,平衡不移动,故D错误。
故选BC。
(2)在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:A(g)+2B(g)![]() 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x,
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x,
A(g)+2B(g)![]() 2C(g)
2C(g)
起始(mol) n 2n 0
转化(mol)nx 2nx 2nx
平衡(mol)n-nx 2n-2nx 2nx
平衡浓度为,c(A)= (n-nx)/Vmol/L,c(B)= (2n-2nx)/Vmol/L,c(C)= 2nx/Vmol/L,
平衡常数K=(2nx/V)2/[( n-nx)/V×(2n-2nx)2/V2]= Vx2/n(1-x)3 ,增大容器体积时,c(B)和c(C)等比例减小,由于A的浓度不变,此时c2(C)/[c(A)c2(B)]的值仍然等于K,所以平衡不移动,故答案为:Vx2/n(1-x)3;C。
(3)由于纵坐标只表示υ逆,为了便于求解,在解题时可把υ正补上;
①该反应是一个反应前后气体体积减小的且正反应是放热的化学反应,t2时逆反应速率突然增大,后逐渐减小达到新平衡,且新平衡时反应速率大于原平衡时反应速率,平衡向逆反应方向移动,改变的条件为增大生成物C的浓度或升高温度,t8时平衡不移动,采用的条件是使用了催化剂。故答案为:升温或增大C的浓度;使用催化剂。
②t2时逆反应速率突然增大,后逐渐减小达到新平衡,且新平衡时反应速率大于原平衡时反应速率,平衡向逆反应方向移动,故答案为:逆反应。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。请完成下列填空:
实验编号 | 待测盐酸的体积(mL) | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) |
1 | 20.00 | 0.10 | 24.18 |
2 | 20.00 | 0.10 | 23.06 |
3 | 20.00 | 0.10 | 22.96 |
(1)根据上述数据,可计算出该盐酸的浓度约为_______________(保留四位有效数字)。
(2)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。
A.用酸式滴定管取20.00 mL待测盐酸,使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(3)氧化还原滴定实验同中和滴定类似,指的是用已知浓度的氧化剂(还原剂)溶液滴定未知浓度的还原剂(氧化剂)溶液。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色H2C2O4溶液。反应离子方程式是_________________________________,滴定达到终点的标志是___________________________________________________。
【题目】BaCl2可用于电子、仪表等工业。以毒重石(主要成分为BaCO3,含少量的CaCO3、MgSO4、Fe2O3、SiO2等杂质)为原料,模拟工业制取BaCl2·2H2O的流程如下图所示:

已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.0 | 3.7 |
(1)盐酸浸取时需要适当加热的原因是_____。
(2)滤渣Ⅰ的成分为_____。
(3)加入H2C2O4时应避免过量,其原因是_____。
(4)用37%的盐酸配制15%的盐酸需用到的仪器有_____(填字母)。
A.量筒 B.烧杯 C.容量瓶 D.玻璃棒
(5)滤渣Ⅲ需经过洗涤后才能进行后续加工处理的原因是_____。
(6)请补充完整由碳酸钡石(含30%CaCO3的BaCO3矿石)模拟工业制取BaCl2·2H2O的实验步骤为_____,过滤,用无水乙醇洗涤2~3次,低温干燥。(实验中可使用的试剂有:冷水,80℃热水,0.1mol·L-1盐酸,6mol·L-1盐酸)