题目内容
【题目】下列有关叙述正确的是( )
A.相同条件下,质量相等的CO和CO2它们所含的氧原子数目之比为11:7
B.同体积、同密度的C2H4和CO,两种气体的分子数一定相等
C.配制450mL0.1molL-1的NaOH溶液,用托盘天平称取NaOH固体1.8g
D.1L0.45molL-1NaCl溶液中Cl-的物质的量浓度比0.1L0.1 molL-1AlCl3溶液大
【答案】BD
【解析】
A.质量相等的CO和CO2的物质的量分别是![]() 、
、![]() ,它们所含的氧原子数目之比为(
,它们所含的氧原子数目之比为(![]() ×1):(
×1):( ![]() ×2)=11:14,故A错误;
×2)=11:14,故A错误;
B. 同体积、同密度的C2H4和CO,质量一定相同,则C2H4和CO的物质的量分别是![]() 、
、![]() ,所以两种气体的分子数一定相等,故B正确;
,所以两种气体的分子数一定相等,故B正确;
C. 配制450mL0.1molL-1的NaOH溶液,需用500 mL容量瓶,需取NaOH固体的质量是0.5L×0.1molL-1×40g/mol=2.0g,故C错误;
D. 1L0.45molL-1NaCl溶液中Cl-的物质的量浓度是0.45molL-1, 0.1L0.1 molL-1AlCl3溶液中Cl-的物质的量浓度是0.3molL-1,故D正确;
答案选BD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】三硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子,某化学兴趣小组对Na2CS3的一些性质进行了探究性实验。
实验Ⅰ.探究Na2CS3的性质:
步骤 | 操作及现象 |
① | 取少量Na2CS3固体溶于蒸馏水中,配制成溶液并分成两等份 |
② | 向其中一份溶液中滴加几滴酚酞试剂,溶液变成红色 |
③ | 向另一份溶液中滴加用硫酸酸化的KMnO4溶液,紫色褪去 |
(1)H2CS3是___(填“强”或“弱”)酸。
(2)已知步骤③中反应的氧化产物是SO42-,则该反应的离子方程式为:____。
(3)某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测定产生的白色沉淀的质量即可求出实验中所用的Na2CS3的质量。你是否同意他的观点,并说明理由:___。
实验Ⅱ.测定Na2CS3溶液的浓度:
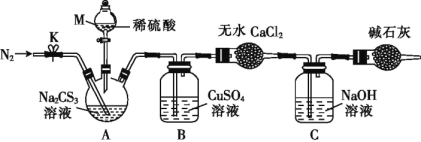
按如图所示装置进行实验:将50.0mLNa2CS3溶液置于三颈烧瓶中,打开仪器M的活塞,滴入足量2.0mol·L-1的稀H2SO4,关闭活塞。
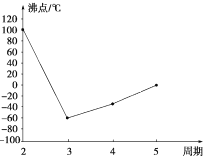
已知:CS32- +2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(4)仪器M的名称是___。反应开始前需要先通入一段时间N2,其作用为____。
(5)B中发生反应的离子方程式为:____。
(6)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉淀质量之前需要进行的实验操作是___。若B中生成沉淀的质量为8.4g,则Na2CS3溶液的物质的量浓度是____。