题目内容
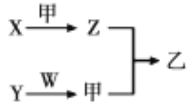
【题目】短周期元素A、B、C、D的原子序数依次增大。X、Y、Z、W分别是由这四种元素中的两种组成的常见化合物,Y为淡黄色固体,W为常见液体;甲为单质,乙为红棕色气体;上述物质之间的转化关系如图所示(部分生成物已省略)。则下列说法中不正确的是
A. 沸点:W>X
B. 原子半径:D>B>C>A
C. C、D两种元素组成的化合物只含有离子键
D. A、B、C三种元素组成的化合物既可以是离子化合物,又可以是共价化合物
【答案】C
【解析】
乙为红棕色气体,乙是NO2 ;Y为淡黄色固体,Y是Na2O2;Y与W生成甲,所以甲是O2,W是常见液体则为H2O,甲与Z生成NO2,所以Z是NO ;X与O2生产NO2,所以X是NH3;因为A、B、C、D的原子序数依次增加,所以分别是H、N、O、Na;综上所述,A、B、C、D分别是H、N、O、Na;X是NH3,Y是Na2O2,Z是NO,W是H2O,甲是O2,乙是NO2。
A. 常温下,W为水液态,X为氨气气态,沸点:W>X,故A正确;
B. 电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:D>B>C>A,故B正确;
C. 氧化钠中只含有离子键,过氧化钠中既有离子键,又含有共价键,故C错误;
D. H、N、O三种元素可组成硝酸,为共价化合物,又可组成硝酸铵,为离子化合物,故D正确;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目