题目内容
19.下列各组化合物中,化学键类型完全相同的是( )| A. | Na2O 和Na2O2 | B. | CaCl2 和 Na2S | C. | CO2 和 CaO | D. | HCl 和NaOH |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.Na2O中只含离子键,Na2O2中含离子键和O-O非极性共价键,故A不选;
B.CaCl2 和 Na2S中,均只含离子键,故B选;
C.CO2中含共价键,CaO中只含离子键,故C不选;
D.HCl中只含共价键,NaOH中含离子键和O-H极性共价键,故D不选;
故选B.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
9.在2L密闭容器中,发生3A(g)+B(g)?2C(g)的反应,若最初加入A和B都是4mol,A的平均反应速率为0.12mol•L-1•s-1,则10s后容器中B的物质的量是( )
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
10.有关如图所示原电池(盐桥中装有含琼脂的KCl饱和溶液)的叙述,正确的是( )


| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 铜离子在铜片表面被还原 | |
| C. | 电流从锌片经导线流向铜片 | |
| D. | 反应中,盐桥中的K+会移向ZnSO4溶液 |
7.化学变化中,反应物的总能量低于生成物的总能量的是( )
| A. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | CaO+H2O=Ca(OH)2 | |
| C. | CaCO3 $\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ | |
| D. | CH3CH2OH(酒精)+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3 H2O |
4.下列说法或做法中正确的是( )
| A. | 氟氯烃的大量排放是造成酸雨的主要原因 | |
| B. | 等质量的同种煤粉和煤块完全燃烧,放出热量前者大于后者 | |
| C. | 液氯泄漏事故发生时,周边的人应该朝顺风方向逃逸或向避风的沟塘低洼处转移 | |
| D. | 火箭发动机有偏二甲肼(C2H8N2)与N2O4混合后充分燃烧,可生成CO2、N2和H2O |
8.下列依据相关实验得出的结论正确的是( )
| A. | 将某无色气体通入品红溶液中,品红溶液褪色,则此气体一定是SO2 | |
| B. | 取少许某溶液并滴加数滴硫氰化钾溶液,无明显现象,再滴加数滴H2O2溶液,溶液变血红色,则原溶液中一定含Fe2+ | |
| C. | 在硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产生,说明Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 在淀粉溶液中加入稀硫酸并加热片刻再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 |
13.元素周期表中某区域的一些元素可用于制造耐高温耐腐蚀合金材料,它们是( )
| A. | 左下方区域的金属元素 | B. | 金属和非金属分界线附近的元素 | ||
| C. | 过渡元素 | D. | 稀有气体元素 |
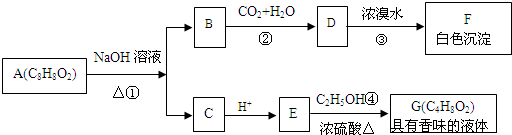
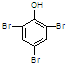 ;
;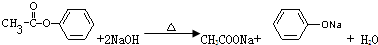 ;
;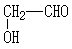 .
.