题目内容
4.下列说法或做法中正确的是( )| A. | 氟氯烃的大量排放是造成酸雨的主要原因 | |
| B. | 等质量的同种煤粉和煤块完全燃烧,放出热量前者大于后者 | |
| C. | 液氯泄漏事故发生时,周边的人应该朝顺风方向逃逸或向避风的沟塘低洼处转移 | |
| D. | 火箭发动机有偏二甲肼(C2H8N2)与N2O4混合后充分燃烧,可生成CO2、N2和H2O |
分析 A.酸雨与N、S的氧化物有关;
B.煤粉和煤块接触面积不同,燃烧速率不同,质量、状态与反应放出热量有关;
C.氯气的密度比空气大;
D.偏二甲肼(C2H8N2)与N2O4混合后充分燃烧,生成稳定的无毒物质.
解答 解:A.酸雨与N、S的氧化物有关,与氟氯烃的大量排放无关,而氟氯烃的大量排放会破坏臭氧空洞,故A错误;
B.煤粉和煤块接触面积不同,燃烧速率不同,质量、状态与反应放出热量有关,则等质量的同种煤粉和煤块完全燃烧,放出热量相同,故B错误;
C.氯气的密度比空气大,则液氯泄漏事故发生时,周边的人应该朝逆风方向逃逸或向避风的高处转移,故C错误;
D.偏二甲肼(C2H8N2)与N2O4混合后充分燃烧,生成稳定的无毒物质,由元素守恒可知生成CO2、N2和H2O,故D正确;
故选D.
点评 本题考查较综合,涉及酸雨、有机物的结构与性质、反应热等,注重高频考点的考查,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
15.关于硫的叙述正确的是( )
| A. | 硫的非金属性较强,所以只以化合态存在于自然界 | |
| B. | 分离黑火药(S、C、KNO3)的成分需要使用二硫化碳、水及过滤操作 | |
| C. | 硫与金属或非金属反应时均做氧化剂 | |
| D. | 1.6克硫与6.4克铜反应能得到8.0克纯净硫化物 |
12.在下列物质中,既含离子键又含共价键的是( )
| A. | MgCl2 | B. | NaOH | C. | H2O | D. | Cl2 |
19.下列各组化合物中,化学键类型完全相同的是( )
| A. | Na2O 和Na2O2 | B. | CaCl2 和 Na2S | C. | CO2 和 CaO | D. | HCl 和NaOH |
16.下列叙述中,正确的是( )
| A. | 用10ml的量筒准确量取8.80ml的稀硫酸 | |
| B. | 用NaOH溶液作标准液滴定未知浓度的醋酸,选择甲基橙做指示剂 | |
| C. | 测定中和反应的热反应,将碱缓慢倒入酸中,所测温度值不变 | |
| D. | 氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
13.下列说法不正确的是( )
| A. | Al箔插入稀HNO3中无现象因Al箔表面被HNO3氧化,形成致密的氧化膜 | |
| B. | “硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触 | |
| C. | “中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,必须干燥或润洗后方可使用 | |
| D. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
18.某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
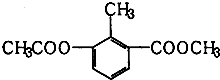

| A. | 一个分子中含有12个H原子 | B. | 该物质属于芳香族化合物 | ||
| C. | 能使酸性KMnO4溶液褪色 | D. | 苯环上的一氯代物有2种 |
 如图表示一个电解池,a是饱和NaCl溶液;X、Y都是石墨电极,U形管内滴入了几滴酚酞试液.请回答以下问题:
如图表示一个电解池,a是饱和NaCl溶液;X、Y都是石墨电极,U形管内滴入了几滴酚酞试液.请回答以下问题: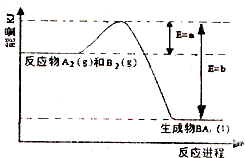 原子序数依次增大的A、B、C、D、E五种短周期元素,A是原子半径最小的元素,B的单质分子中有三对共用电子,C最外层电子数是次外层电子数的3倍,A、D同主族,E原子电子数比C原子电子数多5个,请回答下列问题:
原子序数依次增大的A、B、C、D、E五种短周期元素,A是原子半径最小的元素,B的单质分子中有三对共用电子,C最外层电子数是次外层电子数的3倍,A、D同主族,E原子电子数比C原子电子数多5个,请回答下列问题: ,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O;
,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O;